PRP ທີ່ທັນສະໄຫມ: "PRP ທາງດ້ານການຊ່ວຍ"
ໃນ 10 ປີທີ່ຜ່ານມາ, ໂຄງການການປິ່ນປົວຂອງ PRP ໄດ້ມີການປ່ຽນແປງຢ່າງຫຼວງຫຼາຍ.ໂດຍຜ່ານການທົດລອງແລະການຄົ້ນຄວ້າທາງດ້ານການຊ່ວຍ, ໃນປັດຈຸບັນພວກເຮົາມີຄວາມເຂົ້າໃຈດີຂຶ້ນກ່ຽວກັບ platelet ແລະ physiology ຈຸລັງອື່ນໆ.ນອກຈາກນັ້ນ, ການປະເມີນລະບົບທີ່ມີຄຸນນະພາບສູງຫຼາຍ, ການວິເຄາະ meta ແລະການທົດລອງຄວບຄຸມແບບສຸ່ມໄດ້ສະແດງໃຫ້ເຫັນເຖິງປະສິດທິພາບຂອງເຕັກໂນໂລຢີຊີວະພາບ PRP ໃນຫຼາຍໆດ້ານການແພດ, ລວມທັງຜິວຫນັງ, ການຜ່າຕັດຫົວໃຈ, ການຜ່າຕັດພາດສະຕິກ, ການຜ່າຕັດກະດູກສັນຫຼັງ, ການຄຸ້ມຄອງຄວາມເຈັບປວດ, ພະຍາດກະດູກສັນຫຼັງ, ແລະຢາກິລາ. .
ລັກສະນະໃນປະຈຸບັນຂອງ PRP ແມ່ນຄວາມເຂັ້ມຂົ້ນຂອງ platelet ຢ່າງແທ້ຈິງ, ເຊິ່ງປ່ຽນຈາກຄໍານິຍາມເບື້ອງຕົ້ນຂອງ PRP (ລວມທັງຄວາມເຂັ້ມຂົ້ນຂອງ platelet ສູງກວ່າຄ່າພື້ນຖານ) ຫຼາຍກວ່າ 1 × 10 6 / µ L ຫຼືປະມານ 5 ເທົ່າຂອງຄວາມເຂັ້ມຂົ້ນຂອງ platelet ຕ່ໍາສຸດໃນ platelets ຈາກ. ພື້ນຖານ.ໃນການທົບທວນຄືນຢ່າງກວ້າງຂວາງໂດຍ Fadadu et al.33 ລະບົບ PRP ແລະໂປໂຕຄອນໄດ້ຖືກປະເມີນ.ຈໍານວນ platelet ຂອງການກະກຽມ PRP ສຸດທ້າຍທີ່ຜະລິດໂດຍບາງລະບົບເຫຼົ່ານີ້ແມ່ນຕ່ໍາກວ່າເລືອດທັງຫມົດ.ພວກເຂົາເຈົ້າໄດ້ລາຍງານວ່າປັດໄຈ platelet ຂອງ PRP ເພີ່ມຂຶ້ນຕ່ໍາເປັນ 0.52 ກັບຊຸດ spin ດຽວ (Selphyl ®).ໃນທາງກົງກັນຂ້າມ, ການຫມຸນສອງຄັ້ງ EmCyte Genesis PurePRPII ® ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ທີ່ຜະລິດໂດຍອຸປະກອນແມ່ນສູງສຸດ (1.6 × 10 6 /µL).
ແນ່ນອນ, ວິທີການໃນ vitro ແລະສັດບໍ່ແມ່ນສະພາບແວດລ້ອມການຄົ້ນຄວ້າທີ່ເຫມາະສົມສໍາລັບການຫັນປ່ຽນສົບຜົນສໍາເລັດໄປສູ່ການປະຕິບັດທາງດ້ານການຊ່ວຍ.ເຊັ່ນດຽວກັນ, ການສຶກສາການປຽບທຽບອຸປະກອນບໍ່ສະຫນັບສະຫນູນການຕັດສິນໃຈ, ເພາະວ່າພວກເຂົາສະແດງໃຫ້ເຫັນວ່າຄວາມເຂັ້ມຂົ້ນຂອງ platelet ລະຫວ່າງອຸປະກອນ PRP ແມ່ນແຕກຕ່າງກັນຫຼາຍ.ໂຊກດີ, ໂດຍຜ່ານເຕັກໂນໂລຢີແລະການວິເຄາະໂດຍອີງໃສ່ proteomics, ພວກເຮົາສາມາດເພີ່ມຄວາມເຂົ້າໃຈຂອງພວກເຮົາກ່ຽວກັບຫນ້າທີ່ຂອງເຊນໃນ PRP ທີ່ມີຜົນກະທົບຕໍ່ຜົນການປິ່ນປົວ.ກ່ອນທີ່ຈະບັນລຸຄວາມເຫັນດີເຫັນພ້ອມກ່ຽວກັບການກະກຽມແລະສູດ PRP ມາດຕະຖານ, PRP ຄວນປະຕິບັດຕາມສູດ PRP ທາງດ້ານການຊ່ວຍເພື່ອສົ່ງເສີມກົນໄກການສ້ອມແປງເນື້ອເຍື່ອຢ່າງຫຼວງຫຼາຍແລະຜົນໄດ້ຮັບທາງດ້ານຄລີນິກທີ່ກ້າວຫນ້າ.
ສູດ PRP ທາງຄລີນິກ
ໃນປັດຈຸບັນ, PRP ທາງດ້ານການຊ່ວຍທີ່ມີປະສິດທິພາບ (C-PRP) ໄດ້ຖືກສະແດງວ່າເປັນອົງປະກອບສະລັບສັບຊ້ອນຂອງອົງປະກອບ multicellular autologous ໃນ plasma ປະລິມານຂະຫນາດນ້ອຍທີ່ໄດ້ຮັບຈາກສ່ວນຫນຶ່ງຂອງເລືອດ peripheral ຫຼັງຈາກ centrifugation.ຫຼັງຈາກ centrifugation, PRP ແລະອົງປະກອບຂອງຈຸລັງທີ່ບໍ່ແມ່ນ platelet ສາມາດຟື້ນຕົວຈາກອຸປະກອນຄວາມເຂັ້ມຂົ້ນຕາມຄວາມຫນາແຫນ້ນຂອງຈຸລັງທີ່ແຕກຕ່າງກັນ (ເຊິ່ງຄວາມຫນາແຫນ້ນຂອງ platelet ແມ່ນຕໍ່າສຸດ).
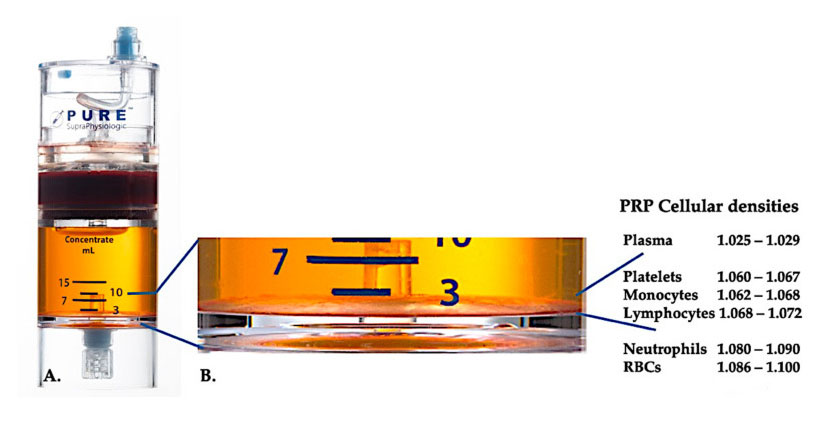
ໃຊ້ອຸປະກອນແຍກຄວາມຫນາແຫນ້ນຂອງຈຸລັງ PurePRP-SP ® (EmCyte Corporation, Fort Myers, FL, USA) ໄດ້ຖືກນໍາໃຊ້ສໍາລັບເລືອດທັງຫມົດຫຼັງຈາກສອງຂັ້ນຕອນການ centrifugation.ຫຼັງຈາກຂະບວນການ centrifugation ທໍາອິດ, ອົງປະກອບຂອງເລືອດທັງຫມົດໄດ້ຖືກແຍກອອກເປັນສອງຊັ້ນພື້ນຖານ, platelet (lean) suspension plasma ແລະຊັ້ນເມັດເລືອດແດງ.ໃນ A, ຂັ້ນຕອນການ centrifugation ທີສອງໄດ້ຖືກສໍາເລັດແລ້ວ.ປະລິມານ PRP ຕົວຈິງສາມາດສະກັດໄດ້ສໍາລັບຄໍາຮ້ອງສະຫມັກຂອງຄົນເຈັບ.ການຂະຫຍາຍໃຫຍ່ຂື້ນໃນ B ສະແດງໃຫ້ເຫັນວ່າມີຊັ້ນສີນ້ໍາຕານການຕົກຕະກອນ erythrocyte ຫຼາຍອົງປະກອບ (ສະແດງໂດຍເສັ້ນສີຟ້າ) ຢູ່ດ້ານລຸ່ມຂອງອຸປະກອນ, ເຊິ່ງປະກອບດ້ວຍຄວາມເຂັ້ມຂົ້ນສູງຂອງ platelets, monocytes ແລະ lymphocytes, ໂດຍອີງໃສ່ gradient ຄວາມຫນາແຫນ້ນ.ໃນຕົວຢ່າງນີ້, ອີງຕາມໂປໂຕຄອນການກະກຽມ C-PRP ກັບ neutrophils ທີ່ບໍ່ດີ, ອັດຕາສ່ວນຕໍ່າສຸດຂອງ neutrophils (<0.3%) ແລະ erythrocytes (<0.1%) ຈະຖືກສະກັດ.
ເມັດເມັດ
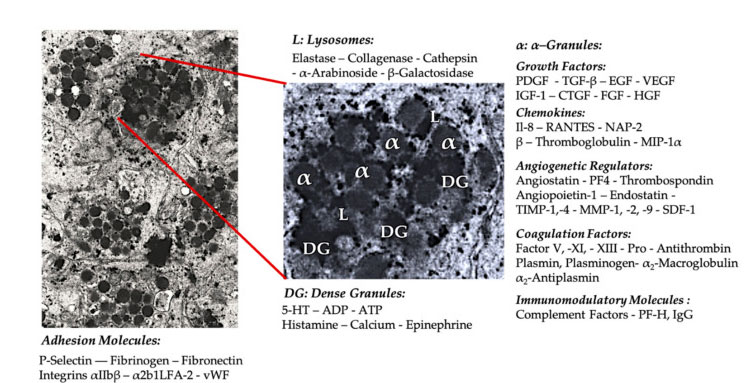
ໃນຄໍາຮ້ອງສະຫມັກ PRP ທາງດ້ານການຊ່ວຍເບື້ອງຕົ້ນ, α- Granules ແມ່ນໂຄງສ້າງພາຍໃນ platelet ທີ່ຖືກກ່າວເຖິງທົ່ວໄປທີ່ສຸດ, ເພາະວ່າພວກມັນປະກອບດ້ວຍປັດໃຈການ coagulation, ຈໍານວນຂະຫນາດໃຫຍ່ຂອງ PDGF ແລະການຄວບຄຸມ angiogenic, ແຕ່ມີຫນ້າທີ່ thrombogenic ຫນ້ອຍ.ປັດໃຈອື່ນໆລວມມີອົງປະກອບຂອງ chemokine ແລະ cytokine ທີ່ຮູ້ຈັກຫນ້ອຍ, ເຊັ່ນ: ປັດໃຈ platelet 4 (PF4), ທາດໂປຼຕີນພື້ນຖານ pre-platelet, P-selectin (ຕົວກະຕຸ້ນຂອງ integrin) ແລະ chemokine RANTES (ຄວບຄຸມໂດຍການກະຕຸ້ນ, ສະແດງອອກ T cells ປົກກະຕິແລະສົມມຸດຕິຖານ. ຄວາມລັບ).ຫນ້າທີ່ໂດຍລວມຂອງອົງປະກອບ granule platelet ສະເພາະເຫຼົ່ານີ້ແມ່ນການທົດແທນແລະກະຕຸ້ນຈຸລັງພູມຕ້ານທານອື່ນໆຫຼືເຮັດໃຫ້ເກີດການອັກເສບຂອງຈຸລັງ endothelial.
ອົງປະກອບຂອງເມັດທີ່ມີຄວາມຫນາແຫນ້ນເຊັ່ນ ADP, serotonin, polyphosphate, histamine ແລະ adrenaline ແມ່ນຖືກນໍາໃຊ້ຫຼາຍ implicitly ເປັນຜູ້ຄວບຄຸມການກະຕຸ້ນຂອງ platelet ແລະ thrombosis.ສໍາຄັນທີ່ສຸດ, ອົງປະກອບເຫຼົ່ານີ້ຈໍານວນຫຼາຍມີຫນ້າທີ່ຂອງການແກ້ໄຂຈຸລັງພູມຕ້ານທານ.Platelet ADP ຖືກຮັບຮູ້ໂດຍ P2Y12ADP receptor ໃນຈຸລັງ dendritic (DC), ດັ່ງນັ້ນການເພີ່ມ endocytosis antigen.DC (antigen presenting cell) ແມ່ນມີຄວາມສໍາຄັນຫຼາຍສໍາລັບການລິເລີ່ມການຕອບສະຫນອງພູມຕ້ານທານຂອງຈຸລັງ T ແລະຄວບຄຸມການຕອບສະຫນອງຂອງພູມຕ້ານທານປ້ອງກັນ, ເຊິ່ງເຊື່ອມຕໍ່ລະບົບພູມຕ້ານທານພາຍໃນແລະລະບົບພູມຕ້ານທານທີ່ປັບຕົວໄດ້.ນອກຈາກນັ້ນ, platelet adenosine triphosphate (ATP) ສົ່ງສັນຍານຜ່ານ T cell receptor P2X7, ນໍາໄປສູ່ການເພີ່ມຄວາມແຕກຕ່າງຂອງຈຸລັງ CD4 T helper ເຂົ້າໄປໃນຈຸລັງ proinflammatory T helper 17 (Th17).ອົງປະກອບຂອງເມັດທີ່ຫນາແຫນ້ນຂອງ platelet ອື່ນໆ (ເຊັ່ນ: glutamate ແລະ serotonin) ເຮັດໃຫ້ເກີດການເຄື່ອນຍ້າຍ T cell ແລະເພີ່ມຄວາມແຕກຕ່າງຂອງ monocyte ກັບ DC, ຕາມລໍາດັບ.ໃນ PRP, immunomodulators ເຫຼົ່ານີ້ໄດ້ມາຈາກອະນຸພາກຫນາແຫນ້ນແມ່ນອຸດົມສົມບູນສູງແລະມີຫນ້າທີ່ຂອງພູມຕ້ານທານຢ່າງຫຼວງຫຼາຍ.
ຈໍານວນຂອງການໂຕ້ຕອບທີ່ມີທ່າແຮງໂດຍກົງແລະທາງອ້ອມລະຫວ່າງ platelets ແລະຈຸລັງ (receptor) ອື່ນໆແມ່ນກວ້າງຂວາງ.ດັ່ງນັ້ນ, ຄໍາຮ້ອງສະຫມັກຂອງ PRP ໃນສະພາບແວດລ້ອມເນື້ອເຍື່ອ pathological ທ້ອງຖິ່ນສາມາດເຮັດໃຫ້ເກີດຄວາມຫລາກຫລາຍຂອງຜົນກະທົບອັກເສບ.
ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet
C-PRP ຄວນມີປະລິມານທາງຄລີນິກຂອງ platelets ເຂັ້ມຂຸ້ນເພື່ອຜະລິດຜົນກະທົບດ້ານການປິ່ນປົວທີ່ເປັນປະໂຫຍດ.Platelets ໃນ C-PRP ຄວນກະຕຸ້ນການຂະຫຍາຍຈຸລັງ, ການສັງເຄາະຂອງ mesenchymal ແລະ neurotrophic ປັດໃຈ, ສົ່ງເສີມການເຄື່ອນຍ້າຍຂອງຈຸລັງ chemotactic ແລະກະຕຸ້ນກິດຈະກໍາ immunoregulatory, ດັ່ງທີ່ສະແດງຢູ່ໃນຮູບ.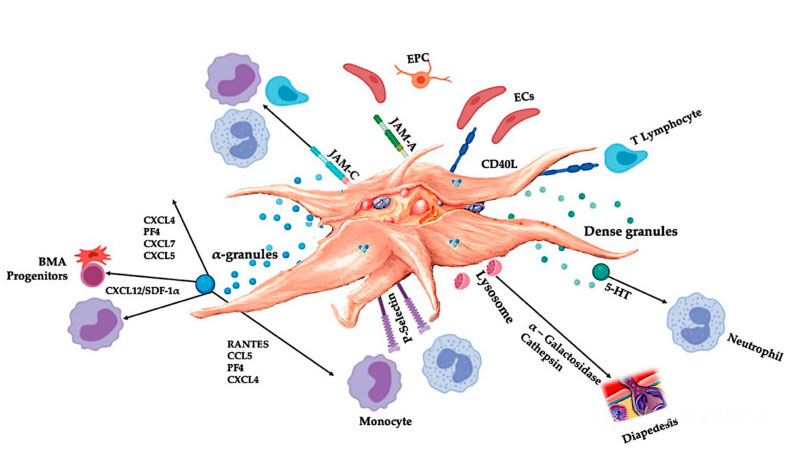
platelets ກະຕຸ້ນ, ການປ່ອຍຂອງ PGF ແລະໂມເລກຸນ adhesion ໄກ່ເກ່ຍຄວາມຫລາກຫລາຍຂອງປະຕິສໍາພັນຂອງເຊນ: chemotaxis, ການຍຶດຕິດຂອງເຊນ, ການເຄື່ອນຍ້າຍ, ແລະຄວາມແຕກຕ່າງຂອງເຊນ, ແລະຄວບຄຸມກິດຈະກໍາຂອງລະບົບພູມຕ້ານທານ.ປະຕິສໍາພັນຂອງຈຸລັງ platelet ເຫຼົ່ານີ້ປະກອບສ່ວນກັບ angiogenesis ແລະກິດຈະກໍາອັກເສບ, ແລະໃນທີ່ສຸດກະຕຸ້ນຂະບວນການສ້ອມແປງເນື້ອເຍື່ອ.ຕົວຫຍໍ້: BMA: ໄຂກະດູກ aspirate, EPC: ຈຸລັງ endothelial progenitor, EC: ຈຸລັງ endothelial, 5-HT: 5-hydroxytryptamine, RANTES: ລະບຽບການກະຕຸ້ນການສະແດງອອກຂອງ T cell ປົກກະຕິແລະການ secretion putative, JAM: junction adhesion ປະເພດໂມເລກຸນ, CD40L: ກຸ່ມ. 40 ligand, SDF-1 α: Stromal cell-derived factor-1 α, CXCL: chemokine (CXC motif) ligand, PF4: platelet factor 4. Adapted from Everts et al.
Marx ແມ່ນຜູ້ທໍາອິດທີ່ພິສູດວ່າການປິ່ນປົວຂອງກະດູກແລະເນື້ອເຍື່ອອ່ອນໄດ້ຖືກປັບປຸງ, ແລະຈໍານວນ platelet ຕ່ໍາສຸດແມ່ນ 1 × 10 6 /µL. ຜົນໄດ້ຮັບເຫຼົ່ານີ້ຖືກຢືນຢັນໃນການສຶກສາຂອງ lumbar fusion ຜ່ານ intervertebral foramen, ເມື່ອປະລິມານ platelet ສູງກວ່າ. 1.3 × ຢູ່ທີ່ 106 platelets/µL, ການສຶກສານີ້ສະແດງໃຫ້ເຫັນເຖິງ fusion ຫຼາຍ.ນອກຈາກນັ້ນ, Giusti et al.ເປີດເຜີຍ 1.5 × ກົນໄກການສ້ອມແປງເນື້ອເຍື່ອໃນປະລິມານ 109 ຕ້ອງການ platelets/mL ເພື່ອກະຕຸ້ນການເກີດ angiogenesis ທີ່ເປັນປະໂຫຍດໂດຍຜ່ານການເຄື່ອນໄຫວຂອງຈຸລັງ endothelial.ໃນການສຶກສາຄັ້ງສຸດທ້າຍ, ຄວາມເຂັ້ມຂຸ້ນທີ່ສູງຂຶ້ນຫຼຸດລົງທ່າແຮງ angiogenesis ຂອງ platelets ໃນແລະອ້ອມ follicles.ນອກຈາກນັ້ນ, ຂໍ້ມູນກ່ອນຫນ້ານີ້ໄດ້ສະແດງໃຫ້ເຫັນວ່າປະລິມານຂອງ PRP ຍັງຈະມີຜົນກະທົບຕໍ່ຜົນການປິ່ນປົວ.ດັ່ງນັ້ນ, ເພື່ອເຮັດໃຫ້ປະຕິກິລິຢາ angiogenesis ຢ່າງຫຼວງຫຼາຍແລະກະຕຸ້ນການຂະຫຍາຍເຊນແລະການເຄື່ອນຍ້າຍຂອງເຊນ, C-PRP ຄວນມີຢ່າງຫນ້ອຍ 7.5 ໃນຂວດການປິ່ນປົວ PRP 5 ມລ × 10 9 ສາມາດສົ່ງເມັດເລືອດອອກໄດ້.
ນອກເຫນືອຈາກການຂື້ນກັບປະລິມານຢາ, ຜົນກະທົບຂອງ PRP ໃນກິດຈະກໍາຂອງເຊນເບິ່ງຄືວ່າແມ່ນຂຶ້ນກັບເວລາສູງ.Sophie et al.ຜົນໄດ້ຮັບເຫຼົ່ານີ້ຊີ້ໃຫ້ເຫັນວ່າການສໍາຜັດໄລຍະສັ້ນກັບ lysates platelet ຂອງມະນຸດສາມາດກະຕຸ້ນການຂະຫຍາຍຈຸລັງກະດູກແລະ chemotaxis.ໃນທາງກົງກັນຂ້າມ, ການສໍາຜັດກັບ PRP ໄລຍະຍາວຈະນໍາໄປສູ່ລະດັບຕ່ໍາຂອງ phosphatase ດ່າງແລະການສ້າງແຮ່ທາດ.
ເມັດເລືອດແດງ
ເມັດເລືອດແດງມີຄວາມຮັບຜິດຊອບໃນການຂົນສົ່ງອົກຊີເຈນໄປສູ່ເນື້ອເຍື່ອແລະການໂອນຄາບອນໄດອອກໄຊຈາກເນື້ອເຍື່ອໄປສູ່ປອດ.ພວກມັນບໍ່ມີແກນ ແລະປະກອບດ້ວຍໂມເລກຸນ heme ທີ່ຜູກມັດກັບໂປຣຕີນ.ອົງປະກອບຂອງທາດເຫຼັກແລະ heme ໃນເມັດເລືອດແດງສົ່ງເສີມການປະສົມປະສານຂອງອົກຊີເຈນແລະຄາບອນໄດອອກໄຊ.ໂດຍທົ່ວໄປ, ວົງຈອນຊີວິດຂອງເມັດເລືອດແດງແມ່ນປະມານ 120 ມື້.ພວກມັນຖືກໂຍກຍ້າຍອອກຈາກການໄຫຼວຽນຂອງ macrophages ຜ່ານຂະບວນການທີ່ເອີ້ນວ່າ RBC aging.ເມັດເລືອດແດງໃນຕົວຢ່າງ PRP ອາດຈະຖືກທໍາລາຍພາຍໃຕ້ເງື່ອນໄຂ shear (ຕົວຢ່າງເຊັ່ນ, ການຜ່າຕັດເລືອດອອກທັງຫມົດ, ຂະບວນການຂອງພູມຕ້ານທານ, ຄວາມກົດດັນ oxidative ຫຼືໂຄງການຄວາມເຂັ້ມຂົ້ນ PRP ທີ່ບໍ່ພຽງພໍ).ດັ່ງນັ້ນ, ເຍື່ອຈຸລັງ RBC ຈະທໍາລາຍແລະປ່ອຍ hemoglobin ທີ່ເປັນພິດ (Hb), ວັດແທກໂດຍ plasma hemoglobin (PFH), heme ແລະທາດເຫຼັກ.].PFH ແລະຜະລິດຕະພັນການເຊື່ອມໂຊມຂອງມັນ (heme ແລະທາດເຫຼັກ) ຮ່ວມກັນນໍາໄປສູ່ການເປັນອັນຕະລາຍແລະຜົນກະທົບ cytotoxic ໃນເນື້ອເຍື່ອ, ນໍາໄປສູ່ຄວາມກົດດັນ oxidative, ການສູນເສຍຂອງ nitric oxide, ການກະຕຸ້ນຂອງເສັ້ນທາງການອັກເສບແລະພູມຕ້ານທານ.ຜົນກະທົບເຫຼົ່ານີ້ໃນທີ່ສຸດກໍ່ຈະເຮັດໃຫ້ເກີດຄວາມຜິດປົກກະຕິຂອງ microcirculation, vasoconstriction ທ້ອງຖິ່ນແລະການບາດເຈັບຂອງ vascular, ເຊັ່ນດຽວກັນກັບຄວາມເສຍຫາຍຂອງເນື້ອເຍື່ອທີ່ຮ້າຍແຮງ.
ສິ່ງທີ່ສໍາຄັນທີ່ສຸດແມ່ນວ່າເມື່ອ RBC ທີ່ມີ C-PRP ຖືກສົ່ງໄປຫາເນື້ອເຍື່ອ, ມັນຈະເຮັດໃຫ້ເກີດປະຕິກິລິຢາທ້ອງຖິ່ນທີ່ເອີ້ນວ່າ eryptosis, ເຊິ່ງຈະເຮັດໃຫ້ການປ່ອຍຕົວຂອງ cytokine ທີ່ມີປະສິດທິພາບແລະ inhibitor ການເຄື່ອນຍ້າຍ macrophage.cytokine ນີ້ຂັດຂວາງການເຄື່ອນຍ້າຍຂອງ monocytes ແລະ macrophages.ມັນອອກສັນຍານສົ່ງເສີມການອັກເສບທີ່ເຂັ້ມແຂງຕໍ່ກັບເນື້ອເຍື່ອອ້ອມຂ້າງ, ຍັບຍັ້ງການເຄື່ອນຍ້າຍຂອງເຊນລໍາຕົ້ນແລະການຂະຫຍາຍຕົວຂອງ fibroblast, ແລະນໍາໄປສູ່ຄວາມຜິດປົກກະຕິຂອງເຊນທ້ອງຖິ່ນທີ່ສໍາຄັນ.ດັ່ງນັ້ນ, ມັນເປັນສິ່ງສໍາຄັນທີ່ຈະຈໍາກັດການປົນເປື້ອນ RBC ໃນການກະກຽມ PRP.ນອກຈາກນັ້ນ, ບົດບາດຂອງເມັດເລືອດແດງໃນການຟື້ນຟູເນື້ອເຍື່ອບໍ່ເຄີຍຖືກກໍານົດ.C-PRP centrifugation ພຽງພໍແລະຂະບວນການກະກຽມໂດຍປົກກະຕິຈະຫຼຸດຜ່ອນຫຼືແມ້ກະທັ້ງການລົບລ້າງການມີເມັດເລືອດແດງ, ດັ່ງນັ້ນຈຶ່ງຫຼີກເວັ້ນຜົນສະທ້ອນທາງລົບຂອງ hemolysis ແລະ polycythemia.
Leukocytes ໃນ C-PRP
ການປະກົດຕົວຂອງເມັດເລືອດຂາວໃນການກະກຽມ PRP ແມ່ນຂຶ້ນກັບອຸປະກອນການປິ່ນປົວແລະລະບົບການກະກຽມ.ໃນອຸປະກອນ PRP ທີ່ອີງໃສ່ plasma, ເມັດເລືອດຂາວຖືກລົບລ້າງຫມົດ;ຢ່າງໃດກໍ່ຕາມ, ເມັດເລືອດຂາວມີຄວາມເຂັ້ມຂຸ້ນຢ່າງຫຼວງຫຼາຍໃນການກະກຽມ PRP ຂອງຊັ້ນສີນ້ໍາຕານ erythrocyte sedimentation.ເນື່ອງຈາກກົນໄກການປ້ອງກັນພູມຕ້ານທານແລະເຈົ້າພາບ, ເມັດເລືອດຂາວມີຜົນກະທົບຢ່າງຫຼວງຫຼາຍຕໍ່ຊີວະວິທະຍາພາຍໃນຂອງສະພາບເນື້ອເຍື່ອສ້ວຍແຫຼມແລະຊໍາເຮື້ອ.ລັກສະນະເຫຼົ່ານີ້ຈະໄດ້ຮັບການປຶກສາຫາລືຕື່ມອີກຂ້າງລຸ່ມນີ້.ດັ່ງນັ້ນ, ການປະກົດຕົວຂອງ leukocytes ສະເພາະໃນ C-PRP ສາມາດເຮັດໃຫ້ເກີດຜົນກະທົບຂອງຈຸລັງແລະເນື້ອເຍື່ອທີ່ສໍາຄັນ.ໂດຍສະເພາະ, ທີ່ແຕກຕ່າງກັນ PRP erythrocyte sedimentation ລະບົບຊັ້ນສີນ້ໍາຕານ - ສີເຫຼືອງໃຊ້ແຜນການກະກຽມທີ່ແຕກຕ່າງກັນ, ດັ່ງນັ້ນການຜະລິດອັດຕາສ່ວນທີ່ແຕກຕ່າງກັນຂອງ neutrophils, lymphocytes ແລະ monocytes ໃນ PRP.Eosinophils ແລະ basophils ບໍ່ສາມາດວັດແທກໄດ້ໃນການກະກຽມ PRP ເພາະວ່າເຍື່ອຈຸລັງຂອງພວກມັນມີຄວາມອ່ອນແອເກີນໄປທີ່ຈະທົນທານຕໍ່ກໍາລັງປະມວນຜົນຂອງສູນກາງ.
Neutrophils
Neutrophils ແມ່ນ leukocytes ທີ່ສໍາຄັນໃນຫຼາຍເສັ້ນທາງການປິ່ນປົວ.ເສັ້ນທາງເຫຼົ່ານີ້ສົມທົບກັບທາດໂປຼຕີນຈາກຕ້ານເຊື້ອຈຸລິນຊີທີ່ມີຢູ່ໃນ platelets ເພື່ອສ້າງເປັນອຸປະສັກທີ່ຫນາແຫນ້ນຕໍ່ກັບເຊື້ອພະຍາດທີ່ຮຸກຮານ.ການມີຢູ່ຂອງ neutrophils ແມ່ນຖືກກໍານົດຕາມເປົ້າຫມາຍການປິ່ນປົວຂອງ C-PRP.ລະດັບການອັກເສບຂອງເນື້ອເຍື່ອເພີ່ມຂຶ້ນອາດຈະຕ້ອງການໃນການປິ່ນປົວບາດແຜຊໍາເຮື້ອ PRP biotherapy ຫຼືໃນຄໍາຮ້ອງສະຫມັກທີ່ແນໃສ່ການຂະຫຍາຍຕົວຂອງກະດູກຫຼືການປິ່ນປົວ.ທີ່ສໍາຄັນ, ຫນ້າທີ່ neutrophil ເພີ່ມເຕີມໄດ້ຖືກພົບເຫັນຢູ່ໃນຫຼາຍແບບ, ເນັ້ນຫນັກໃສ່ບົດບາດຂອງພວກເຂົາໃນ angiogenesis ແລະການສ້ອມແປງເນື້ອເຍື່ອ.ຢ່າງໃດກໍ່ຕາມ, neutrophils ຍັງສາມາດເຮັດໃຫ້ເກີດຜົນກະທົບທີ່ເປັນອັນຕະລາຍ, ດັ່ງນັ້ນພວກມັນບໍ່ເຫມາະສົມສໍາລັບບາງຄໍາຮ້ອງສະຫມັກ.Zhou ແລະ Wang ໄດ້ພິສູດວ່າການນໍາໃຊ້ PRP ອຸດົມສົມບູນໃນ neutrophils ສາມາດນໍາໄປສູ່ການເພີ່ມຂຶ້ນໃນອັດຕາສ່ວນຂອງ collagen ປະເພດ III ກັບ collagen ປະເພດ I, ດັ່ງນັ້ນ exacerbating fibrosis ແລະຫຼຸດຜ່ອນຄວາມເຂັ້ມແຂງ tendon.ລັກສະນະທີ່ເປັນອັນຕະລາຍອື່ນໆທີ່ໄກ່ເກ່ຍໂດຍ neutrophils ແມ່ນການປ່ອຍ cytokines ອັກເສບແລະ matrix metalloproteinases (MMPs), ເຊິ່ງສາມາດສົ່ງເສີມການອັກເສບແລະ catabolism ເມື່ອນໍາໃຊ້ກັບແພຈຸລັງ.
Leukomonocyte
ໃນ C-PRP, mononuclear T ແລະ B lymphocytes ແມ່ນເຂັ້ມຂຸ້ນຫຼາຍກ່ວາເມັດເລືອດຂາວອື່ນໆ.ພວກມັນມີຄວາມກ່ຽວຂ້ອງຢ່າງໃກ້ຊິດກັບພູມຕ້ານທານການປັບຕົວ cytotoxic ຂອງຈຸລັງ.Lymphocytes ສາມາດກະຕຸ້ນປະຕິກິລິຍາຂອງເຊນເພື່ອຕໍ່ສູ້ກັບການຕິດເຊື້ອແລະປັບຕົວເຂົ້າກັບຜູ້ບຸກລຸກ.ນອກຈາກນັ້ນ, cytokines ທີ່ມາຈາກ T-lymphocyte (interferon- γ [IFN- γ] ແລະ interleukin-4 (IL-4)) ເສີມຂະຫຍາຍ polarization ຂອງ macrophages. ຮູບແບບຫນູໂດຍການຄວບຄຸມຄວາມແຕກຕ່າງຂອງ monocytes ແລະ macrophages.
Monocyte - ເຊນສ້ອມແປງທີ່ມີທ່າແຮງຫຼາຍ
ອີງຕາມອຸປະກອນການກະກຽມ PRP ທີ່ໃຊ້, monocytes ອາດຈະ protrude ຫຼືບໍ່ມີຢູ່ໃນຂວດການປິ່ນປົວ PRP.ແຕ່ຫນ້າເສຍດາຍ, ການປະຕິບັດແລະຄວາມສາມາດໃນການຟື້ນຟູຂອງພວກເຂົາແມ່ນບໍ່ຄ່ອຍຖືກກ່າວເຖິງໃນວັນນະຄະດີ.ດັ່ງນັ້ນ, ຄວາມສົນໃຈພຽງເລັກນ້ອຍແມ່ນຈ່າຍໃຫ້ກັບ monocytes ໃນວິທີການກະກຽມຫຼືສູດສຸດທ້າຍ.ກຸ່ມ Monocyte ມີຄວາມແຕກຕ່າງກັນ, ມີຕົ້ນກຳເນີດມາຈາກຈຸລັງ progenitor ໃນໄຂກະດູກ, ແລະຖືກສົ່ງໄປຫາເນື້ອເຍື່ອ peripheral ຜ່ານທາງຈຸລັງ ລຳ ຕົ້ນຂອງ hematopoietic ຕາມການກະຕຸ້ນ microenvironment.ໃນລະຫວ່າງການ homeostasis ແລະການອັກເສບ, monocytes ໄຫຼອອກຈາກກະແສເລືອດແລະຖືກບັນຈຸເຂົ້າໄປໃນເນື້ອເຍື່ອທີ່ບາດເຈັບຫຼືຊຸດໂຊມ.ພວກເຂົາສາມາດປະຕິບັດເປັນ macrophages (M Φ) ຈຸລັງ Effector ຫຼືຈຸລັງ progenitor.ຈຸລັງ monocytes, macrophages ແລະ dendritic ເປັນຕົວແທນຂອງລະບົບ phagocytic mononuclear (MPS).ຢູ່ໃນເນື້ອເຍື່ອທີ່ເສື່ອມໂຊມ, macrophages ທີ່ຢູ່ອາໃສ, ປັດໄຈການຂະຫຍາຍຕົວໃນທ້ອງຖິ່ນ, cytokines ທີ່ສົ່ງເສີມການອັກເສບ, ຈຸລັງ apoptotic ຫຼື necrotic ແລະຜະລິດຕະພັນຈຸລິນຊີລິເລີ່ມ monocytes ເພື່ອຄວາມແຕກຕ່າງໃນກຸ່ມຈຸລັງ MPS.ສົມມຸດວ່າເມື່ອ C-PRP ບັນຈຸ monocytes ທີ່ມີຜົນຜະລິດສູງຖືກສີດເຂົ້າໄປໃນ microenvironment ທ້ອງຖິ່ນຂອງພະຍາດ, monocytes ມີແນວໂນ້ມທີ່ຈະແຕກຕ່າງກັນເປັນ M Φເພື່ອເຮັດໃຫ້ເກີດການປ່ຽນແປງຂອງເຊນໃຫຍ່.
ຈາກ monocyte ກັບ M Φໃນຂະບວນການຂອງການຫັນເປັນ, ສະເພາະ M Φ Phenotype.ໃນສິບປີທີ່ຜ່ານມາ, ຮູບແບບຫນຶ່ງໄດ້ຖືກພັດທະນາ, ເຊິ່ງປະສົມປະສານ M Φ ກົນໄກການກະຕຸ້ນທີ່ຊັບຊ້ອນໄດ້ຖືກອະທິບາຍວ່າເປັນ polarization ຂອງສອງລັດກົງກັນຂ້າມ: M Φ Phenotype 1 (M Φ 1, ການກະຕຸ້ນແບບຄລາສສິກ) ແລະ M Φ Phenotype 2 (M Φ. 2, ການກະຕຸ້ນທາງເລືອກ).M Φ 1 ມີລັກສະນະອັກເສບ cytokine secretion (IFN- γ) ແລະ nitric oxide ການຜະລິດກົນໄກການຂ້າເຊື້ອພະຍາດປະສິດທິພາບ.M Φ phenotype ຍັງຜະລິດປັດໄຈການຂະຫຍາຍຕົວຂອງ endothelial vascular (VEGF) ແລະປັດໄຈການຂະຫຍາຍຕົວ fibroblast (FGF).M Φ phenotype ແມ່ນປະກອບດ້ວຍຈຸລັງຕ້ານການອັກເສບທີ່ມີ phagocytosis ສູງ.M Φ 2 ຜະລິດອົງປະກອບ matrix extracellular, angiogenesis ແລະ chemokines, ແລະ interleukin 10 (IL-10).ນອກເຫນືອໄປຈາກການປ້ອງກັນເຊື້ອພະຍາດ, M Φມັນຍັງສາມາດຫຼຸດຜ່ອນການອັກເສບແລະສົ່ງເສີມການສ້ອມແປງເນື້ອເຍື່ອ.ເປັນທີ່ສັງເກດວ່າ M Φ 2 ໄດ້ຖືກແບ່ງອອກເປັນ M in vitro Φ 2a, M Φ 2b ແລະ M Φ 2. ມັນຂຶ້ນກັບການກະຕຸ້ນ.ໃນ vivo ການແປພາສາຂອງປະເພດຍ່ອຍເຫຼົ່ານີ້ແມ່ນມີຄວາມຫຍຸ້ງຍາກເພາະວ່າເນື້ອເຍື່ອອາດຈະປະກອບດ້ວຍກຸ່ມ M Φປະສົມ.ຫນ້າສົນໃຈ, ໂດຍອີງໃສ່ສັນຍານສິ່ງແວດລ້ອມທ້ອງຖິ່ນແລະລະດັບ IL-4, proinflammatory M Φ 1 ສາມາດຖືກປ່ຽນເພື່ອສົ່ງເສີມການສ້ອມແປງ M Φ 2. ຈາກຂໍ້ມູນເຫຼົ່ານີ້, ມັນສົມເຫດສົມຜົນທີ່ຈະສົມມຸດວ່າມີຄວາມເຂັ້ມຂົ້ນສູງຂອງ monocytes ແລະ M Φ C-PRP ການກະກຽມ. ອາດຈະປະກອບສ່ວນໃນການສ້ອມແປງເນື້ອເຍື່ອທີ່ດີກວ່າເພາະວ່າພວກມັນມີການສ້ອມແປງເນື້ອເຍື່ອຕ້ານການອັກເສບແລະຄວາມສາມາດໃນການຖ່າຍທອດສັນຍານຂອງເຊນ.
ຄໍານິຍາມທີ່ສັບສົນຂອງສ່ວນຫນຶ່ງຂອງເມັດເລືອດຂາວໃນ PRP
ການປະກົດຕົວຂອງເມັດເລືອດຂາວໃນຂວດການປິ່ນປົວ PRP ແມ່ນຂຶ້ນກັບອຸປະກອນການກະກຽມ PRP ແລະອາດມີຄວາມແຕກຕ່າງຢ່າງຫຼວງຫຼາຍ.ມີຫຼາຍຂໍ້ຂັດແຍ່ງກ່ຽວກັບການມີຢູ່ຂອງ leukocytes ແລະການປະກອບສ່ວນຂອງເຂົາເຈົ້າກັບຜະລິດຕະພັນຍ່ອຍ PRP ທີ່ແຕກຕ່າງກັນ (ເຊັ່ນ: PRGF, P-PRP, LP-PRP, LR-PRP, P-PRF ແລະ L-PRF) ໃນການທົບທວນຄືນທີ່ຜ່ານມາ, ຫົກ randomized. ການທົດລອງຄວບຄຸມ (ຫຼັກຖານລະດັບ 1) ແລະສາມການສຶກສາປຽບທຽບໃນອະນາຄົດ (ຫຼັກຖານລະດັບ 2) ກ່ຽວຂ້ອງກັບຄົນເຈັບ 1055, ຊີ້ໃຫ້ເຫັນວ່າ LR-PRP ແລະ LP-PRP ມີຄວາມປອດໄພທີ່ຄ້າຍຄືກັນ.ຜູ້ຂຽນໄດ້ສະຫຼຸບວ່າປະຕິກິລິຍາທາງລົບຂອງ PRP ອາດຈະບໍ່ກ່ຽວຂ້ອງໂດຍກົງກັບຄວາມເຂັ້ມຂົ້ນຂອງເມັດເລືອດຂາວ.ໃນການສຶກສາອື່ນ, LR-PRP ບໍ່ໄດ້ປ່ຽນແປງການອັກເສບ interleukin (IL-1) ໃນຫົວເຂົ່າ OA, IL-6, IL-8 ແລະ IL-17).ຜົນໄດ້ຮັບເຫຼົ່ານີ້ສະຫນັບສະຫນູນທັດສະນະວ່າບົດບາດຂອງ leukocytes ໃນກິດຈະກໍາທາງຊີວະພາບຂອງ PRP ໃນ vivo ອາດຈະມາຈາກ crosstalk ລະຫວ່າງ platelets ແລະ leukocytes.ປະຕິສໍາພັນນີ້ສາມາດສົ່ງເສີມການ biosynthesis ຂອງປັດໃຈອື່ນໆ (ເຊັ່ນ: lipoxygen), ເຊິ່ງສາມາດຊົດເຊີຍຫຼືສົ່ງເສີມການ regression ຂອງການອັກເສບ.ຫຼັງຈາກການປ່ອຍຕົວເບື້ອງຕົ້ນຂອງໂມເລກຸນອັກເສບ (ອາຊິດ arachidonic, leukotriene ແລະ prostaglandin), lipoxygen A4 ຖືກປ່ອຍອອກມາຈາກ platelets ກະຕຸ້ນເພື່ອປ້ອງກັນການກະຕຸ້ນ neutrophil.ມັນແມ່ນຢູ່ໃນສະພາບແວດລ້ອມນີ້ທີ່ M Φ Phenotype ຈາກ M Φ 1 ປ່ຽນເປັນ M Φ 2. ນອກຈາກນັ້ນ, ຍັງມີຫຼັກຖານທີ່ເພີ່ມຂຶ້ນວ່າການແຜ່ກະຈາຍຂອງຈຸລັງ mononuclear ສາມາດແຍກອອກເປັນຊະນິດຂອງຈຸລັງທີ່ບໍ່ແມ່ນ phagocytic ເນື່ອງຈາກ pluripotency ຂອງມັນ.
ປະເພດຂອງ PRP ຈະສົ່ງຜົນກະທົບຕໍ່ວັດທະນະທໍາ MSC.ເມື່ອປຽບທຽບກັບຕົວຢ່າງ PRP ຫຼື PPP ບໍລິສຸດ, LR-PRP ສາມາດເຮັດໃຫ້ເກີດການແຜ່ຂະຫຍາຍຂອງກະດູກທີ່ມາຈາກ MSCs (BMMSCs), ມີການປ່ອຍຕົວໄວຂຶ້ນແລະກິດຈະກໍາທາງຊີວະພາບ PGF ທີ່ດີຂຶ້ນ.ຄຸນລັກສະນະທັງ ໝົດ ເຫຼົ່ານີ້ແມ່ນສະດວກຕໍ່ການເພີ່ມ monocytes ເຂົ້າໄປໃນຂວດການປິ່ນປົວ PRP ແລະຮັບຮູ້ຄວາມສາມາດຂອງ immunomodulatory ແລະທ່າແຮງທີ່ແຕກຕ່າງກັນ.
ລະບຽບການພູມຕ້ານທານແຕ່ກໍາເນີດແລະການປັບຕົວຂອງ PRP
ຫນ້າທີ່ທາງກາຍະພາບທີ່ມີຊື່ສຽງທີ່ສຸດຂອງ platelets ແມ່ນການຄວບຄຸມເລືອດ.ພວກມັນສະສົມຢູ່ບ່ອນທໍາລາຍເນື້ອເຍື່ອແລະເສັ້ນເລືອດທີ່ເສຍຫາຍ.ເຫດການເຫຼົ່ານີ້ແມ່ນເກີດມາຈາກການສະແດງອອກຂອງ integrins ແລະ selectins ທີ່ກະຕຸ້ນໃຫ້ platelet adhesion ແລະການລວບລວມ.endothelium ທີ່ເສຍຫາຍເຮັດໃຫ້ຂະບວນການນີ້ຮ້າຍແຮງຂຶ້ນ, ແລະ collagen ທີ່ຖືກເປີດເຜີຍແລະໂປຣຕີນ subendothelial matrix ອື່ນໆສົ່ງເສີມການກະຕຸ້ນເລິກຂອງ platelets.ໃນກໍລະນີເຫຼົ່ານີ້, ບົດບາດສໍາຄັນຂອງການພົວພັນລະຫວ່າງປັດໄຈ von Willebrand (vWF) ແລະ glycoprotein (GP), ໂດຍສະເພາະແມ່ນ GP-Ib, ໄດ້ຖືກພິສູດແລ້ວ.ຫຼັງຈາກການກະຕຸ້ນຂອງ platelet, platelet α-、 Dense, lysosome ແລະ T-granules ຄວບຄຸມ exocytosis ແລະປ່ອຍເນື້ອໃນຂອງມັນເຂົ້າໄປໃນສະພາບແວດລ້ອມ extracellular.
ໂມເລກຸນການຍຶດຕິດຂອງເມັດ
ເພື່ອເຂົ້າໃຈບົດບາດຂອງ PRP ໃນເນື້ອເຍື່ອອັກເສບແລະ platelets ໃນການຕອບສະຫນອງຂອງພູມຕ້ານທານ, ພວກເຮົາຄວນຈະເຂົ້າໃຈວິທີການທີ່ແຕກຕ່າງກັນຂອງ receptors ດ້ານ platelet (integrins) ແລະ junction adhesion molecules (JAM) ແລະປະຕິສໍາພັນຂອງເຊນສາມາດເລີ່ມຕົ້ນຂະບວນການທີ່ສໍາຄັນໃນພູມຕ້ານທານ innate ແລະປັບຕົວໄດ້.
Integrins ແມ່ນໂມເລກຸນການຍຶດຕິດຂອງເຊນທີ່ພົບເຫັນຢູ່ໃນປະເພດຕ່າງໆຂອງເຊນແລະສະແດງອອກໃນປະລິມານຫຼາຍໃນ platelets.Integrins ລວມມີ a5b1, a6b1, a2b1 LFA-2, (GPIa/IIa) ແລະ aIIbb3 (GPIIb/IIIa).ໂດຍປົກກະຕິແລ້ວ, ພວກມັນຢູ່ໃນສະຖານະຄົງທີ່ ແລະມີຄວາມສຳພັນຕໍ່າ.ຫຼັງຈາກການກະຕຸ້ນ, ພວກເຂົາເຈົ້າສະຫຼັບກັບສະຖານະຂອງການຜູກມັດ ligand ສູງ.Integrins ມີຫນ້າທີ່ທີ່ແຕກຕ່າງກັນກ່ຽວກັບ platelets ແລະມີສ່ວນຮ່ວມໃນການໂຕ້ຕອບຂອງ platelets ກັບຫຼາຍໆຊະນິດຂອງເມັດເລືອດຂາວ, ຈຸລັງ endothelial ແລະ extracellular matrix.ນອກຈາກນັ້ນ, ສະລັບສັບຊ້ອນ GP-Ib-V-IX ແມ່ນສະແດງອອກໃນເຍື່ອ platelet ແລະເປັນ receptor ຕົ້ນຕໍສໍາລັບການຜູກມັດກັບ von vWF.ປະຕິສໍາພັນນີ້ໄກ່ເກ່ຍການຕິດຕໍ່ເບື້ອງຕົ້ນລະຫວ່າງ platelets ແລະໂຄງສ້າງ subendothelial ທີ່ຖືກເປີດເຜີຍ.Platelet integrin ແລະ GP complex ແມ່ນກ່ຽວຂ້ອງກັບຂະບວນການອັກເສບຕ່າງໆແລະມີບົດບາດສໍາຄັນໃນການສ້າງສະລັບສັບຊ້ອນ platelet-leucocyte.ໂດຍສະເພາະ, integrin aIIbb3 ແມ່ນມີຄວາມຈໍາເປັນເພື່ອສ້າງສະລັບສັບຊ້ອນທີ່ຫມັ້ນຄົງໂດຍການສົມທົບ fibrinogen ກັບ macrophage 1 antigen (Mac-1) receptor ສຸດ neutrophils.
Platelets, neutrophils ແລະຈຸລັງ endothelial vascular ສະແດງໂມເລກຸນການຍຶດຕິດຂອງເຊນສະເພາະ, ເອີ້ນວ່າ selectin.ພາຍໃຕ້ສະພາບການອັກເສບ, ເມັດເລືອດສະແດງອອກ P-selectin ແລະ neutrophil L-selectin.ຫຼັງຈາກການກະຕຸ້ນຂອງ platelet, P-selectin ອາດຈະຜູກມັດກັບ ligand PSGL-1 ທີ່ມີຢູ່ໃນ neutrophils ແລະ monocytes.ນອກຈາກນັ້ນ, ການຜູກມັດ PSGL-1 ເລີ່ມຕົ້ນປະຕິກິລິຍາຂອງສັນຍານ intracellular, ເຊິ່ງກະຕຸ້ນ neutrophils ຜ່ານ neutrophil integrin Mac-1 ແລະ lymphocyte function-related antigen 1 (LFA-1).ເປີດໃຊ້ Mac-1 ຜູກມັດກັບ GPIb ຫຼື GPIIb/IIIa ໃນ platelets ຜ່ານ fibrinogen, ດັ່ງນັ້ນຈຶ່ງເຮັດໃຫ້ປະຕິສໍາພັນລະຫວ່າງ neutrophils ແລະ platelets ມີສະຖຽນລະພາບ.ນອກຈາກນັ້ນ, activated LFA-1 ສາມາດສົມທົບກັບ platelet intercellular adhesion molecule 2 ເພື່ອເຮັດໃຫ້ສະຖຽນລະພາບ neutrophil-platelet ເພີ່ມເຕີມເພື່ອສົ່ງເສີມການຍຶດຫມັ້ນໃນໄລຍະຍາວກັບຈຸລັງ.
Platelets ແລະ leukocytes ມີບົດບາດສໍາຄັນໃນການຕອບສະຫນອງພູມຕ້ານທານພາຍໃນແລະປັບຕົວ
ຮ່າງກາຍສາມາດຮັບຮູ້ຮ່າງກາຍຕ່າງປະເທດແລະເນື້ອເຍື່ອທີ່ໄດ້ຮັບບາດເຈັບໃນພະຍາດສ້ວຍແຫຼມຫຼືຊໍາເຮື້ອເພື່ອລິເລີ່ມການປິ່ນປົວບາດແຜບາດແຜແລະເສັ້ນທາງອັກເສບ.ລະບົບພູມຕ້ານທານພາຍໃນແລະປັບຕົວໄດ້ປົກປ້ອງເຈົ້າພາບຈາກການຕິດເຊື້ອ, ແລະເມັດເລືອດຂາວມີບົດບາດສໍາຄັນໃນການຊ້ອນກັນລະຫວ່າງສອງລະບົບ.ໂດຍສະເພາະ, monocytes, macrophages, neutrophils ແລະຈຸລັງ killer ທໍາມະຊາດມີບົດບາດສໍາຄັນໃນລະບົບ innate, ໃນຂະນະທີ່ lymphocytes ແລະ subsets ຂອງເຂົາເຈົ້າມີບົດບາດຄ້າຍຄືກັນໃນລະບົບພູມຕ້ານທານການປັບຕົວ.
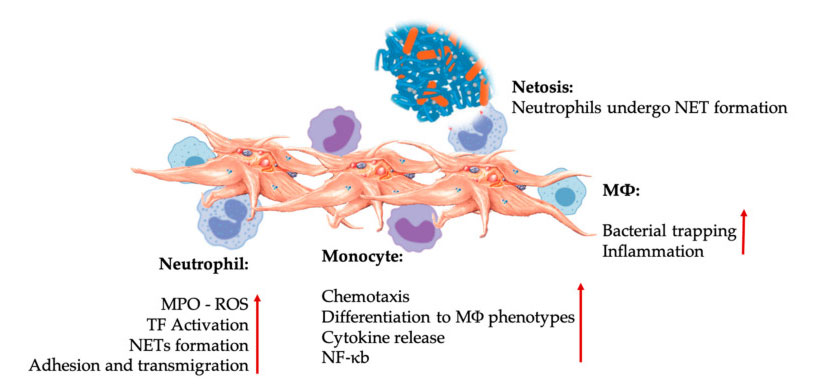
ປະຕິກິລິຍາຂອງ Platelet ແລະ leukocyte ໃນການໂຕ້ຕອບຂອງຈຸລັງພູມຕ້ານທານ.Platelet ພົວພັນກັບ neutrophils ແລະ monocytes, ແລະສຸດທ້າຍດ້ວຍ M Φ Interact, ປັບແລະເພີ່ມຫນ້າທີ່ຂອງ effector.ປະຕິສໍາພັນຂອງ platelet-leucocyte ເຫຼົ່ານີ້ນໍາໄປສູ່ການອັກເສບໂດຍຜ່ານກົນໄກທີ່ແຕກຕ່າງກັນ, ລວມທັງ NETosis.ຕົວຫຍໍ້: MPO: myeloperoxidase, ROS: reactive oxygen species, TF: tissue factor, NET: neutrophil extracellular trap, NF- κ B: Nuclear factor kappa B, M Φ: Macrophages.
ລະບົບພູມຕ້ານທານພາຍໃນ
ພາລະບົດບາດຂອງລະບົບພູມຕ້ານທານພາຍໃນແມ່ນເພື່ອກໍານົດ microorganisms invasive ຫຼືຊິ້ນເນື້ອເຍື່ອທີ່ບໍ່ສະເພາະແລະກະຕຸ້ນການເກັບກູ້ຂອງເຂົາເຈົ້າ.ເມື່ອໂຄງສ້າງໂມເລກຸນທີ່ແນ່ນອນເອີ້ນວ່າ receptors ການຮັບຮູ້ຮູບແບບການສະແດງອອກຂອງພື້ນຜິວ (PRRs) ສົມທົບກັບຮູບແບບໂມເລກຸນທີ່ກ່ຽວຂ້ອງກັບເຊື້ອພະຍາດແລະຮູບແບບໂມເລກຸນທີ່ກ່ຽວຂ້ອງກັບຄວາມເສຍຫາຍ, ລະບົບພູມຕ້ານທານພາຍໃນຈະຖືກເປີດໃຊ້.ມີຫຼາຍປະເພດຂອງ PRRs, ລວມທັງ Toll-like receptor (TLR) ແລະ RIG-1 like receptor (RLR).receptors ເຫຼົ່ານີ້ສາມາດກະຕຸ້ນປັດໄຈ transcription ຕົ້ນຕໍ kappa B (NF- κ B) ມັນຍັງຄວບຄຸມຫຼາຍດ້ານຂອງການຕອບສະຫນອງພູມຕ້ານທານ innate ແລະປັບຕົວໄດ້.ຫນ້າສົນໃຈ, platelets ຍັງສະແດງຄວາມຫລາກຫລາຍຂອງໂມເລກຸນ immunoregulatory receptor ຢູ່ເທິງຫນ້າດິນແລະ cytoplasm, ເຊັ່ນ P-selectin, transmembrane protein CD40 ligand (CD40L), cytokines (ເຊັ່ນ IL-1 β, TGF- β) ແລະ platelet-specific TLR. ດັ່ງນັ້ນ, platelets ສາມາດພົວພັນກັບຈຸລັງພູມຕ້ານທານຕ່າງໆ.
ປະຕິກິລິຍາຂອງເມັດເລືອດຂາວໃນພູມຕ້ານທານພາຍໃນ
ເມື່ອ platelets ເຂົ້າໄປໃນຫຼືບຸກລຸກການໄຫຼຂອງເລືອດຫຼືເນື້ອເຍື່ອ, platelets ແມ່ນຈຸລັງຫນຶ່ງທີ່ກວດພົບການບາດເຈັບ endothelial ແລະເຊື້ອພະຍາດ microbial ກ່ອນ.ການລວບລວມ Platelet ແລະສົ່ງເສີມການປ່ອຍ platelet agonists ADP, thrombin ແລະ vWF, ເຮັດໃຫ້ເກີດການກະຕຸ້ນ platelet ແລະການສະແດງອອກຂອງ platelet chemokine receptors C, CC, CXC ແລະ CX3C, ດັ່ງນັ້ນຈຶ່ງເຮັດໃຫ້ platelets ຢູ່ໃນສະຖານທີ່ຕິດເຊື້ອຫຼືການບາດເຈັບ.
ລະບົບພູມຕ້ານທານພາຍໃນແມ່ນຖືກກໍານົດໄວ້ລ່ວງຫນ້າທາງພັນທຸກໍາເພື່ອກວດພົບຜູ້ບຸກລຸກ, ເຊັ່ນ: ໄວຣັສ, ເຊື້ອແບັກທີເຣັຍ, ແມ່ກາຝາກແລະສານພິດ, ຫຼືບາດແຜເນື້ອເຍື່ອແລະບາດແຜ.ມັນເປັນລະບົບທີ່ບໍ່ສະເພາະ, ເພາະວ່າເຊື້ອພະຍາດໃດໆຈະຖືກລະບຸວ່າເປັນຂອງຕ່າງປະເທດຫຼືບໍ່ແມ່ນຕົວຂອງມັນເອງແລະຕັ້ງຢູ່ຢ່າງໄວວາ.ລະບົບພູມຕ້ານທານພາຍໃນແມ່ນອີງໃສ່ຊຸດຂອງທາດໂປຼຕີນແລະ phagocytes, ເຊິ່ງຮັບຮູ້ຄຸນລັກສະນະທີ່ຮັກສາໄວ້ໄດ້ດີຂອງເຊື້ອພະຍາດແລະກະຕຸ້ນການຕອບສະຫນອງຂອງພູມຕ້ານທານຢ່າງໄວວາເພື່ອຊ່ວຍກໍາຈັດຜູ້ຮຸກຮານ, ເຖິງແມ່ນວ່າເຈົ້າພາບບໍ່ເຄີຍສໍາຜັດກັບເຊື້ອພະຍາດສະເພາະມາກ່ອນ.
Neutrophils, monocytes ແລະຈຸລັງ dendritic ແມ່ນຈຸລັງພູມຕ້ານທານທີ່ພົບເລື້ອຍທີ່ສຸດໃນເລືອດ.ການຈ້າງງານຂອງພວກເຂົາແມ່ນມີຄວາມຈໍາເປັນສໍາລັບການຕອບສະຫນອງພູມຕ້ານທານທີ່ພຽງພໍ.ໃນເວລາທີ່ PRP ຖືກນໍາໃຊ້ໃນຢາປົວພະຍາດຟື້ນຟູ, ປະຕິສໍາພັນຂອງຈຸລັງເມັດສີຂາວຄວບຄຸມການອັກເສບ, ການປິ່ນປົວບາດແຜແລະການສ້ອມແປງເນື້ອເຍື່ອ.TLR-4 ໃນ platelets ກະຕຸ້ນປະຕິສໍາພັນ platelet-neutrophil, ເຊິ່ງຄວບຄຸມອັນທີ່ເອີ້ນວ່າ leukocyte oxidative burst ໂດຍການຄວບຄຸມການປ່ອຍຂອງຊະນິດອົກຊີເຈນທີ່ reactive (ROS) ແລະ myeloperoxidase (MPO) ຈາກ neutrophils.ນອກຈາກນັ້ນ, ການພົວພັນລະຫວ່າງ platelet-neutrophil ແລະ neutrophil degranulation ນໍາໄປສູ່ການສ້າງຕັ້ງຂອງດັກ neutrophil-extracellular (NETs).NETs ແມ່ນປະກອບດ້ວຍແກນ neutrophil ແລະເນື້ອໃນ neutrophil intracellular ອື່ນໆ, ເຊິ່ງສາມາດຈັບເຊື້ອແບັກທີເຣັຍແລະຂ້າພວກມັນຜ່ານ NETosis.ການສ້າງຕັ້ງຂອງ NETs ແມ່ນກົນໄກການຂ້າທີ່ສໍາຄັນຂອງ neutrophils.
ຫຼັງຈາກການກະຕຸ້ນຂອງ platelet, monocytes ສາມາດເຄື່ອນຍ້າຍໄປສູ່ເນື້ອເຍື່ອທີ່ເປັນພະຍາດແລະ degenerative, ບ່ອນທີ່ພວກເຂົາປະຕິບັດກິດຈະກໍາການຍຶດຕິດແລະ secrete ໂມເລກຸນອັກເສບທີ່ອາດຈະມີການປ່ຽນແປງ chemotaxis ແລະຄຸນສົມບັດ proteolytic.ນອກຈາກນັ້ນ, platelets ສາມາດກະຕຸ້ນການກະຕຸ້ນ monocyte NF- κ B ເພື່ອຄວບຄຸມການເຮັດວຽກຂອງ monocytes, ເຊິ່ງເປັນຕົວໄກ່ເກ່ຍທີ່ສໍາຄັນຂອງການຕອບສະຫນອງອັກເສບແລະການກະຕຸ້ນແລະຄວາມແຕກຕ່າງຂອງຈຸລັງພູມຕ້ານທານ.Platelets ສົ່ງເສີມການລະເບີດຂອງ oxidative endogenous ຂອງ monocytes ເພື່ອສົ່ງເສີມການທໍາລາຍເຊື້ອພະຍາດ phagocytic.ການປ່ອຍ MPO ແມ່ນໄກ່ເກ່ຍໂດຍການໂຕ້ຕອບໂດຍກົງລະຫວ່າງ platelet-monocyte CD40L-MAC-1.ຫນ້າສົນໃຈ, ໃນເວລາທີ່ P-selectin activates platelets ພາຍໃຕ້ສະພາບເນື້ອເຍື່ອອັກເສບສ້ວຍແຫຼມແລະຊໍາເຮື້ອ, platelet-derived chemokines PF4, RANTES, IL-1 βແລະ CXCL-12 ສາມາດປ້ອງກັນ apoptosis spontaneous ຂອງ monocytes, ແຕ່ສົ່ງເສີມຄວາມແຕກຕ່າງຂອງພວກມັນເຂົ້າໄປໃນ macrophages.
ລະບົບພູມຕ້ານທານທີ່ປັບຕົວໄດ້
ຫຼັງຈາກລະບົບພູມຕ້ານທານພາຍໃນທີ່ບໍ່ສະເພາະຮັບຮູ້ຄວາມເສຍຫາຍຂອງຈຸລິນຊີຫຼືເນື້ອເຍື່ອ, ລະບົບພູມຕ້ານທານທີ່ປັບຕົວສະເພາະຈະຄອບຄອງ.ລະບົບການປັບຕົວປະກອບມີ antigen-binding B lymphocytes (B cells) ແລະ T lymphocytes ທໍາມະດາ (Treg) ທີ່ປະສານງານການເກັບກູ້ເຊື້ອພະຍາດ.ຈຸລັງ T ສາມາດແບ່ງອອກເປັນຈຸລັງ T ຜູ້ຊ່ວຍ (Th cells) ແລະຈຸລັງ T cytotoxic (ຈຸລັງ Tc, ເຊິ່ງເອີ້ນກັນວ່າຈຸລັງ T killer).ຈຸລັງ Th ໄດ້ຖືກແບ່ງອອກຕື່ມອີກເປັນຈຸລັງ Th1, Th2 ແລະ Th17, ເຊິ່ງມີຫນ້າທີ່ສໍາຄັນໃນການອັກເສບ.ຈຸລັງ Th ສາມາດ secrete cytokines proinflammatory (ເຊັ່ນ: IFN- γ, TNF- β) ແລະ interleukins ຫຼາຍຊະນິດ (ຕົວຢ່າງ, IL-17). ພວກມັນມີປະສິດທິພາບໂດຍສະເພາະໃນການປ້ອງກັນເຊື້ອໄວຣັສ intracellular ແລະເຊື້ອແບັກທີເລຍ. ຈຸລັງ tc ແມ່ນຈຸລັງ effector, ເຊິ່ງສາມາດກໍາຈັດເຊື້ອຈຸລິນຊີພາຍໃນແລະຈຸລັງພາຍນອກທີ່ຖືກເປົ້າຫມາຍ.
ຫນ້າສົນໃຈ, ຈຸລັງ Th2 ຜະລິດ IL-4 ແລະສົ່ງຜົນກະທົບຕໍ່ M Φ Polarization, M Φ ແນະນໍາການຟື້ນຟູ M Φ 2 Phenotype, ໃນຂະນະທີ່ IFN- γ M Φ ການປ່ຽນແປງໄປສູ່ການອັກເສບ M Φ 1 Phenotype, ເຊິ່ງຂຶ້ນກັບປະລິມານແລະເວລາຂອງ cytokines.ຫຼັງຈາກ IL-4 ຖືກເປີດໃຊ້, M Φ 2 induces Treg cells to differentiate into Th2 cells, ແລະຫຼັງຈາກນັ້ນຜະລິດ IL-4 ເພີ່ມເຕີມ (loop ຄວາມຄິດເຫັນໃນທາງບວກ).ຈຸລັງ Th ປ່ຽນ M Φ phenotype ແມ່ນມຸ້ງໄປຫາ phenotype ຟື້ນຟູໃນການຕອບສະຫນອງຕໍ່ຕົວແທນທາງຊີວະພາບຂອງຕົ້ນກໍາເນີດຂອງເນື້ອເຍື່ອ.ກົນໄກນີ້ແມ່ນອີງໃສ່ຫຼັກຖານວ່າຈຸລັງ Th ມີບົດບາດສໍາຄັນໃນການຄວບຄຸມການອັກເສບແລະການສ້ອມແປງເນື້ອເຍື່ອ.
ປະຕິສໍາພັນຂອງເມັດເລືອດຂາວໃນລະບົບພູມຕ້ານທານທີ່ປັບຕົວໄດ້
ລະບົບພູມຕ້ານທານທີ່ປັບຕົວໄດ້ໃຊ້ຕົວຮັບສະເພາະ antigen ແລະຈື່ຈໍາເຊື້ອພະຍາດທີ່ພົບໃນເມື່ອກ່ອນ, ແລະທໍາລາຍພວກມັນເມື່ອມັນພົບກັບເຈົ້າພາບຕໍ່ມາ.ຢ່າງໃດກໍ່ຕາມ, ການຕອບສະຫນອງພູມຕ້ານທານທີ່ປັບຕົວເຫຼົ່ານີ້ພັດທະນາຊ້າໆ.Konias et al.ມັນສະແດງໃຫ້ເຫັນວ່າອົງປະກອບຂອງ platelet ປະກອບສ່ວນກັບການຮັບຮູ້ຄວາມສ່ຽງແລະການສ້ອມແປງເນື້ອເຍື່ອ, ແລະປະຕິສໍາພັນລະຫວ່າງ platelets ແລະ leukocytes ສົ່ງເສີມການກະຕຸ້ນຂອງການຕອບສະຫນອງພູມຕ້ານທານການປັບຕົວ.
ໃນລະຫວ່າງການຕອບສະຫນອງພູມຕ້ານທານທີ່ປັບຕົວໄດ້, platelets ສົ່ງເສີມການຕອບສະຫນອງ monocyte ແລະ macrophage ໂດຍຜ່ານ DC ແລະ NK cell maturation, ນໍາໄປສູ່ການຕອບສະຫນອງສະເພາະຂອງຈຸລັງ T ແລະ B.ດັ່ງນັ້ນ, ອົງປະກອບຂອງເມັດ platelet ມີຜົນກະທົບໂດຍກົງຕໍ່ການປັບຕົວຂອງພູມຕ້ານທານໂດຍການສະແດງອອກຂອງ CD40L, ໂມເລກຸນທີ່ຈໍາເປັນສໍາລັບການຄວບຄຸມການຕອບສະຫນອງຂອງພູມຕ້ານທານ.Platelets ຜ່ານ CD40L ບໍ່ພຽງແຕ່ມີບົດບາດໃນການນໍາສະເຫນີ antigen, ແຕ່ຍັງມີຜົນກະທົບຕໍ່ປະຕິກິລິຍາ T cell.Liu et al.ມັນໄດ້ຖືກພົບເຫັນວ່າ platelets ຄວບຄຸມການຕອບສະຫນອງຂອງ CD4 T cell ໃນວິທີທີ່ສະລັບສັບຊ້ອນ.ລະບຽບການທີ່ແຕກຕ່າງກັນຂອງຊຸດຍ່ອຍຂອງ CD4 T cell ຫມາຍຄວາມວ່າ platelets ສົ່ງເສີມຈຸລັງ CD4 T ເພື່ອຕອບສະຫນອງຕໍ່ການກະຕຸ້ນການອັກເສບ, ດັ່ງນັ້ນຈຶ່ງເຮັດໃຫ້ເກີດການຕອບສະຫນອງທີ່ເຂັ້ມແຂງແລະຕ້ານການອັກເສບ.
Platelets ຍັງຄວບຄຸມການຕອບສະ ໜອງ ຂອງການປັບຕົວຂອງເຊນ B ຕໍ່ກັບເຊື້ອພະຍາດຈຸລິນຊີ.ມັນເປັນທີ່ຮູ້ກັນດີວ່າ CD40L ຢູ່ໃນຈຸລັງ CD4 T ທີ່ຖືກເປີດໃຊ້ຈະກະຕຸ້ນ CD40 ຂອງຈຸລັງ B, ໃຫ້ສັນຍານທີສອງທີ່ຕ້ອງການສໍາລັບການກະຕຸ້ນ B lymphocyte ທີ່ຂຶ້ນກັບ T-cell, ການປ່ຽນ allotype ຕໍ່ມາ, ແລະຄວາມແຕກຕ່າງແລະການຂະຫຍາຍຈຸລັງ B.ໂດຍທົ່ວໄປ, ຜົນໄດ້ຮັບສະແດງໃຫ້ເຫັນຢ່າງຈະແຈ້ງກ່ຽວກັບຫນ້າທີ່ຕ່າງໆຂອງ platelets ໃນການປັບຕົວຂອງພູມຕ້ານທານ, ສະແດງໃຫ້ເຫັນວ່າ platelets ເຊື່ອມຕໍ່ການພົວພັນລະຫວ່າງ T cell ແລະ B cell ຜ່ານ CD40-CD40L, ດັ່ງນັ້ນການເພີ່ມປະສິດທິພາບການຕອບສະຫນອງ B cell ທີ່ຂຶ້ນກັບ T-cell.ນອກຈາກນັ້ນ, platelets ແມ່ນອຸດົມສົມບູນໃນ receptors ພື້ນຜິວຂອງເຊນ, ເຊິ່ງສາມາດສົ່ງເສີມການກະຕຸ້ນ platelet ແລະປ່ອຍຈໍານວນຂະຫນາດໃຫຍ່ຂອງຂະບວນການອັກເສບແລະການເຄື່ອນໄຫວທາງຊີວະພາບເກັບຮັກສາໄວ້ໃນ particles platelet ທີ່ແຕກຕ່າງກັນ, ດັ່ງນັ້ນຜົນກະທົບຕໍ່ການຕອບສະຫນອງຂອງພູມຕ້ານທານ innate ແລະປັບຕົວ.
ການຂະຫຍາຍບົດບາດຂອງ serotonin ທີ່ມາຈາກ platelet ໃນ PRP
Serotonin (5-hydroxytryptamine, 5-HT) ມີບົດບາດສໍາຄັນທີ່ຊັດເຈນໃນລະບົບປະສາດສ່ວນກາງ (CNS), ລວມທັງຄວາມທົນທານຕໍ່ຄວາມເຈັບປວດ.ມັນໄດ້ຖືກຄາດຄະເນວ່າສ່ວນໃຫຍ່ຂອງ 5-HT ຂອງມະນຸດແມ່ນຜະລິດຢູ່ໃນກະເພາະລໍາໄສ້ແລະຫຼັງຈາກນັ້ນໂດຍຜ່ານການໄຫຼວຽນຂອງເລືອດ, ບ່ອນທີ່ມັນຖືກດູດຊຶມໂດຍ platelets ຜ່ານ serotonin reuptake transporter ແລະເກັບຮັກສາໄວ້ໃນອະນຸພາກຫນາແຫນ້ນທີ່ມີຄວາມເຂັ້ມຂົ້ນສູງ (65 mmol / L).5-HT ເປັນ neurotransmitter ທີ່ມີຊື່ສຽງແລະຮໍໂມນທີ່ຊ່ວຍຄວບຄຸມຂະບວນການ neuropsychological ຕ່າງໆໃນ CNS (central 5-HT).ຢ່າງໃດກໍ່ຕາມ, ສ່ວນໃຫຍ່ຂອງ 5-HT ມີຢູ່ພາຍນອກ CNS (peripheral 5-HT), ແລະມັນມີສ່ວນຮ່ວມໃນການຄວບຄຸມການເຮັດວຽກທາງຊີວະພາບຂອງລະບົບແລະຈຸລັງຂອງລະບົບອະໄວຍະວະຕ່າງໆ, ລວມທັງລະບົບ cardiovascular, ປອດ, gastrointestinal, urogenital ແລະ platelet.5-HT ມີຄວາມເຂັ້ມຂົ້ນຂອງ metabolism ຂຶ້ນກັບຊະນິດຂອງຈຸລັງ, ລວມທັງ adipocytes, ຈຸລັງ epithelial ແລະເມັດເລືອດຂາວ.Peripheral 5-HT ຍັງເປັນຕົວຄວບຄຸມພູມຕ້ານທານທີ່ມີປະສິດທິພາບ, ເຊິ່ງສາມາດກະຕຸ້ນຫຼືຍັບຍັ້ງການອັກເສບແລະຜົນກະທົບຕໍ່ຈຸລັງພູມຕ້ານທານຕ່າງໆໂດຍຜ່ານ receptor 5-HT (5HTR).
ກົນໄກ Paracrine ແລະ autocrine ຂອງ HT
ກິດຈະກໍາຂອງ 5-HT ແມ່ນການໄກ່ເກ່ຍໂດຍການໂຕ້ຕອບຂອງມັນກັບ 5HTRs, ເຊິ່ງເປັນ superfamily ທີ່ມີເຈັດສະມາຊິກ (5-HT 1 - 7) ແລະຢ່າງຫນ້ອຍ 14 ຊະນິດຍ່ອຍຂອງ receptor ທີ່ແຕກຕ່າງກັນ, ລວມທັງສະມາຊິກທີ່ຄົ້ນພົບບໍ່ດົນມານີ້ 5-HT 7, ອຸປະກອນຂ້າງຂອງມັນແລະ. ປະຕິບັດຫນ້າທີ່ໃນການຄຸ້ມຄອງຄວາມເຈັບປວດ.ໃນຂະບວນການຂອງ platelet degranulation, platelets activated secrete ຈໍານວນຂະຫນາດໃຫຍ່ຂອງ platelet-derived 5-HT, ເຊິ່ງສາມາດສົ່ງເສີມການຫົດຕົວຂອງ vascular ແລະກະຕຸ້ນການກະຕຸ້ນຂອງ platelets ແລະ lymphocytes ທີ່ຢູ່ໃກ້ຄຽງໂດຍຜ່ານການສະແດງອອກຂອງ 5-HTR ກ່ຽວກັບຈຸລັງ endothelial, ຈຸລັງກ້າມເນື້ອລຽບແລະ. ຈຸລັງພູມຕ້ານທານ.Pacala et al.ຜົນກະທົບ mitotic ຂອງ 5-HT ກ່ຽວກັບຈຸລັງ endothelial vascular ໄດ້ຖືກສຶກສາ, ແລະທ່າແຮງຂອງການສົ່ງເສີມການຂະຫຍາຍຕົວຂອງເສັ້ນເລືອດທີ່ເສຍຫາຍໂດຍການກະຕຸ້ນ angiogenesis ໄດ້ຖືກກໍານົດ.ວິທີການເຫຼົ່ານີ້ຖືກຄວບຄຸມແມ່ນບໍ່ຊັດເຈນ, ແຕ່ມັນອາດຈະກ່ຽວຂ້ອງກັບເສັ້ນທາງສັນຍານສອງທາງທີ່ແຕກຕ່າງກັນໃນ microcircuit ຂອງຈຸລັງເພື່ອຄວບຄຸມການເຮັດວຽກຂອງຈຸລັງ endothelial vascular ແລະຈຸລັງກ້າມຊີ້ນລຽບ, fibroblasts ແລະຈຸລັງພູມຕ້ານທານໂດຍຜ່ານ receptors 5-HT ສະເພາະໃນຈຸລັງເຫຼົ່ານີ້. .ການເຮັດວຽກຂອງ autocrine ຂອງ platelet 5-HT ຫຼັງຈາກການກະຕຸ້ນ platelet ໄດ້ຖືກອະທິບາຍ [REF].ການປ່ອຍຂອງ 5-HT ເສີມຂະຫຍາຍການກະຕຸ້ນຂອງ platelets ແລະການທົດແທນຂອງ platelets ໄຫຼວຽນ, ນໍາໄປສູ່ການກະຕຸ້ນຂອງຕິກິຣິຍາ cascade ສັນຍານແລະ effectors ນ້ໍາສະຫນັບສະຫນູນ platelet reactivity.
ຜົນກະທົບ Immunomodulatory 5-HT
ຫຼັກຖານຫຼາຍກວ່າແລະຫຼາຍສະແດງໃຫ້ເຫັນວ່າ serotonin ສາມາດມີບົດບາດໃນ 5HTR ທີ່ແຕກຕ່າງກັນເປັນຕົວຄວບຄຸມພູມຕ້ານທານ.ອີງຕາມ 5HTR ສະແດງອອກໃນ leukocytes ຕ່າງໆທີ່ກ່ຽວຂ້ອງກັບປະຕິກິລິຢາອັກເສບ, 5-HT ທີ່ມາຈາກ platelet ເຮັດຫນ້າທີ່ເປັນຕົວຄວບຄຸມພູມຕ້ານທານທັງໃນລະບົບພູມຕ້ານທານພາຍໃນແລະການປັບຕົວ.5-HT ສາມາດກະຕຸ້ນການຈະເລີນເຕີບໂຕຂອງ Treg ແລະຄວບຄຸມການເຮັດວຽກຂອງຈຸລັງ B, ຈຸລັງ killer ທໍາມະຊາດແລະ neutrophils ໂດຍການທົດແທນ DC ແລະ monocytes ໄປຫາສະຖານທີ່ອັກເສບ.ການສຶກສາທີ່ຜ່ານມາໄດ້ສະແດງໃຫ້ເຫັນວ່າ platelet-derived 5-HT ສາມາດຄວບຄຸມການເຮັດວຽກຂອງຈຸລັງພູມຕ້ານທານພາຍໃຕ້ເງື່ອນໄຂສະເພາະ.ດັ່ງນັ້ນ, ການນໍາໃຊ້ C-PRP, ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ແມ່ນຫຼາຍກ່ວາ 1 × 10 6 / µ L ຢ່າງຫຼວງຫຼາຍສາມາດຊ່ວຍການຂົນສົ່ງຄວາມເຂັ້ມຂົ້ນຂອງ 5-HT ທີ່ມາຈາກ platelets ຂະຫນາດໃຫຍ່ໄປສູ່ເນື້ອເຍື່ອ.ໃນສະພາບແວດລ້ອມຈຸນລະພາກທີ່ມີລັກສະນະອັກເສບ, PRP ສາມາດພົວພັນກັບຈຸລັງພູມຕ້ານທານຈໍານວນຫນຶ່ງທີ່ມີບົດບາດສໍາຄັນໃນ pathologies ເຫຼົ່ານີ້, ເຊິ່ງອາດຈະສົ່ງຜົນກະທົບຕໍ່ຜົນໄດ້ຮັບທາງດ້ານການຊ່ວຍ.
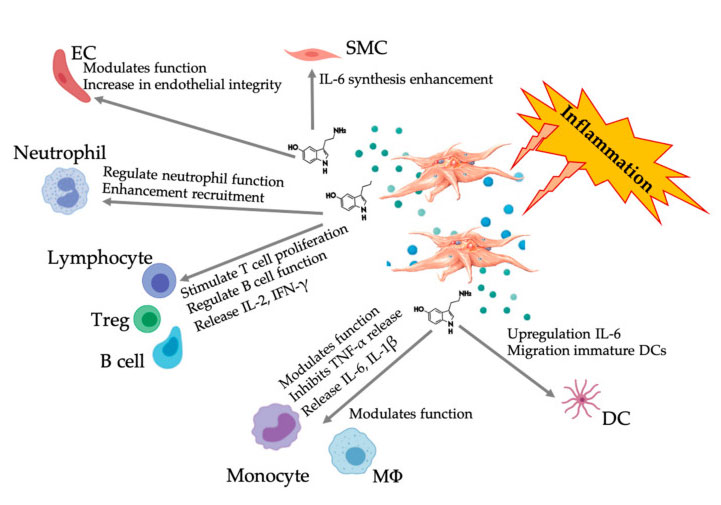
ຮູບສະແດງການຕອບສະ ໜອງ 5-HT multifaceted ຫຼັງຈາກການກະຕຸ້ນຂອງ platelets PRP ອັກເສບ.ຫຼັງຈາກການກະຕຸ້ນຂອງ platelets, platelets ປ່ອຍ granules ຂອງເຂົາເຈົ້າ, ລວມທັງ 5-HT ໃນ granules ຫນາແຫນ້ນ, ເຊິ່ງມີຜົນກະທົບທີ່ແຕກຕ່າງກັນກ່ຽວກັບຈຸລັງພູມຕ້ານທານຕ່າງໆ, ຈຸລັງ endothelial ແລະຈຸລັງກ້າມເນື້ອກ້ຽງ.ຕົວຫຍໍ້: SMC: ຈຸລັງກ້າມເນື້ອລຽບ, EC: ຈຸລັງ endothelial, Treg: T lymphocytes ທໍາມະດາ, M Φ: Macrophages, DC: ຈຸລັງ dendritic, IL: interleukin, IFN- γ: Interferon γ . ດັດແກ້ແລະດັດແປງຈາກ Everts et al.ແລະ Hull et al.
ຜົນກະທົບທາງລົບຂອງ PRP
platelets ກະຕຸ້ນຈະປ່ອຍຕົວໄກ່ເກ່ຍທີ່ສົ່ງເສີມການອັກເສບແລະຕ້ານການອັກເສບຫຼາຍ, ເຊິ່ງບໍ່ພຽງແຕ່ສາມາດເຮັດໃຫ້ເກີດຄວາມເຈັບປວດ, ແຕ່ຍັງຫຼຸດຜ່ອນການອັກເສບແລະຄວາມເຈັບປວດ.ເມື່ອນໍາໃຊ້, ນະໂຍບາຍດ້ານ platelet ປົກກະຕິຂອງ PRP ປ່ຽນແປງ microenvironment ກ່ອນທີ່ຈະສ້ອມແປງເນື້ອເຍື່ອແລະການຟື້ນຟູໂດຍຜ່ານເສັ້ນທາງທີ່ສັບສົນຫຼາຍທີ່ກ່ຽວຂ້ອງກັບ anabolism ແລະ catabolism, ການຂະຫຍາຍຈຸລັງ, ຄວາມແຕກຕ່າງແລະລະບຽບການຂອງຈຸລັງລໍາຕົ້ນ.ຄຸນລັກສະນະເຫຼົ່ານີ້ຂອງ PRP ນໍາໄປສູ່ການນໍາໃຊ້ PRP ໃນເງື່ອນໄຂທາງດ້ານການຊ່ວຍທາງດ້ານການຊ່ວຍຕ່າງໆຕາມປົກກະຕິກັບອາການເຈັບຊໍາເຮື້ອ (ເຊັ່ນ: ການບາດເຈັບກິລາ, ພະຍາດ orthopedic, ພະຍາດກະດູກສັນຫຼັງແລະບາດແຜຊໍາເຮື້ອທີ່ສັບສົນ), ເຖິງແມ່ນວ່າກົນໄກທີ່ແນ່ນອນບໍ່ໄດ້ຖືກກໍານົດຢ່າງເຕັມສ່ວນ.
ໃນປີ 2008, Evertz et al.ມັນເປັນການທົດລອງຄວບຄຸມແບບສຸ່ມຄັ້ງທໍາອິດເພື່ອລາຍງານຜົນກະທົບຂອງຢາແກ້ປວດຂອງການກະກຽມ PRP, ເຊິ່ງໄດ້ຖືກກະກຽມຈາກຊັ້ນສີນ້ໍາຕານຂອງອັດຕາການຕົກຕະກອນ autologous erythrocyte ແລະກະຕຸ້ນດ້ວຍ autologous thrombin ຫຼັງຈາກການຜ່າຕັດບ່າ.ພວກເຂົາເຈົ້າສັງເກດເຫັນການຫຼຸດລົງຢ່າງຫຼວງຫຼາຍໃນຄະແນນການປຽບທຽບສາຍຕາ, ການນໍາໃຊ້ຢາແກ້ປວດໂດຍອີງໃສ່ opioid, ແລະການຟື້ນຕົວຫຼັງການຜ່າຕັດທີ່ປະສົບຜົນສໍາເລັດຫຼາຍຂຶ້ນ.ມັນເປັນທີ່ສັງເກດວ່າພວກມັນສະທ້ອນເຖິງຜົນກະທົບທາງລົບຂອງ platelets activated ແລະຄາດຄະເນກ່ຽວກັບກົນໄກຂອງ platelets ປ່ອຍ 5-HT.ໃນສັ້ນ, platelets ແມ່ນ dormant ໃນ PRP ການກະກຽມສົດ.ຫຼັງຈາກການກະຕຸ້ນຂອງ platelets ໂດຍກົງຫຼືທາງອ້ອມ (ປັດໄຈຂອງເນື້ອເຍື່ອ), platelets ປ່ຽນຮູບຮ່າງແລະຜະລິດທີ່ບໍ່ຖືກຕ້ອງພຽງພໍທີ່ຈະສົ່ງເສີມການລວບລວມ platelet.ຫຼັງຈາກນັ້ນ, ພວກເຂົາເຈົ້າປ່ອຍ intracellular α- ແລະອະນຸພາກຫນາແຫນ້ນ.ເນື້ອເຍື່ອທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ PRP ທີ່ຖືກກະຕຸ້ນຈະຖືກບຸກລຸກໂດຍ PGF, cytokines ແລະ platelet lysosomes ອື່ນໆ.ໂດຍສະເພາະ, ໃນເວລາທີ່ອະນຸພາກຫນາແຫນ້ນປ່ອຍເນື້ອໃນຂອງເຂົາເຈົ້າ, ພວກເຂົາຈະປ່ອຍຈໍານວນຂະຫນາດໃຫຍ່ຂອງ 5-HT ທີ່ຄວບຄຸມຄວາມເຈັບປວດ.ໃນ C-PRP, ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ແມ່ນສູງກວ່າ 5 ຫາ 7 ເທົ່າໃນເລືອດຂ້າງຄຽງ.ດັ່ງນັ້ນ, ການປ່ອຍ 5-HT ຈາກ platelets ແມ່ນດາລາສາດ.ຫນ້າສົນໃຈ, Sprott et al.ບົດລາຍງານໄດ້ສັງເກດເຫັນວ່າອາການເຈັບປວດໄດ້ຖືກບັນເທົາລົງຢ່າງຫຼວງຫຼາຍຫຼັງຈາກການຝັງເຂັມແລະ moxibustion, ຄວາມເຂັ້ມຂົ້ນຂອງ platelet ທີ່ມາຈາກ 5-HT ໄດ້ຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ, ແລະຫຼັງຈາກນັ້ນລະດັບ plasma ຂອງ 5-HT ແມ່ນເພີ່ມຂຶ້ນ.
ຢູ່ໃນອຸປະກອນຂ້າງຄຽງ, platelets, mast cells ແລະ endothelial cell ຈະປ່ອຍ endogenous 5-HT ໃນລະຫວ່າງການບາດເຈັບຂອງເນື້ອເຍື່ອຫຼືການຜ່າຕັດ.ຫນ້າສົນໃຈ, ຄວາມຫລາກຫລາຍຂອງ 5-HT receptors ຂອງ neurons ໄດ້ຖືກກວດພົບຢູ່ໃນພື້ນທີ່ peripheral, ເຊິ່ງຢືນຢັນວ່າ 5-HT ສາມາດແຊກແຊງລະບົບສາຍສົ່ງ nociceptive ໃນເຂດ peripheral.ການສຶກສາເຫຼົ່ານີ້ສະແດງໃຫ້ເຫັນວ່າ 5-HT ສາມາດສົ່ງຜົນກະທົບຕໍ່ການສົ່ງຕໍ່ nociceptive ຂອງແພຈຸລັງ peripheral ຜ່ານ 5-HT1, 5-HT2, 5-HT3, 5-HT4 ແລະ 5-HT7 receptors.
ລະບົບ 5-HT ເປັນຕົວແທນຂອງລະບົບທີ່ມີປະສິດທິພາບທີ່ສາມາດຫຼຸດຜ່ອນແລະເພີ່ມລະດັບຄວາມເຈັບປວດຫຼັງຈາກການກະຕຸ້ນທີ່ເປັນອັນຕະລາຍ.ລະບຽບການສູນກາງແລະ peripheral ຂອງສັນຍານ nociceptive ແລະການປ່ຽນແປງໃນລະບົບ 5-HT ໄດ້ຖືກລາຍງານໃນຄົນເຈັບທີ່ມີອາການເຈັບຊໍາເຮື້ອ.ໃນຊຸມປີມໍ່ໆມານີ້, ການສຶກສາຈໍານວນຫລາຍໄດ້ສຸມໃສ່ບົດບາດຂອງ 5-HT ແລະ receptors ຂອງຕົນໃນການປຸງແຕ່ງແລະຄວບຄຸມຂໍ້ມູນທີ່ເປັນອັນຕະລາຍ, ເຊິ່ງກໍ່ໃຫ້ເກີດຢາເສບຕິດເຊັ່ນ: selective serotonin reuptake inhibitors (SSRI).ຢານີ້ inhibits reuptake ຂອງ serotonin ເຂົ້າໄປໃນ neurons presynaptic ຫຼັງຈາກການປ່ອຍຂອງ serotonin.ມັນມີຜົນກະທົບຕໍ່ໄລຍະເວລາແລະຄວາມເຂັ້ມຂົ້ນຂອງການສື່ສານ serotonin ແລະເປັນການປິ່ນປົວທາງເລືອກສໍາລັບອາການເຈັບຊໍາເຮື້ອ.ການຄົ້ນຄວ້າທາງດ້ານຄລີນິກເພີ່ມເຕີມແມ່ນຈໍາເປັນເພື່ອເຂົ້າໃຈຢ່າງຈະແຈ້ງກ່ຽວກັບກົນໄກໂມເລກຸນຂອງ PRP-derived ກົດລະບຽບອາການເຈັບປວດ 5-HT ໃນພະຍາດຊໍາເຮື້ອແລະ degenerative.
ຂໍ້ມູນອື່ນໆເພື່ອແກ້ໄຂຜົນກະທົບທາງລົບທີ່ມີທ່າແຮງຂອງ PRP ສາມາດໄດ້ຮັບຫຼັງຈາກການທົດສອບຕົວແບບສັດທີ່ມີອາການປວດຮາກ.ການສະຫຼຸບສະຖິຕິປຽບທຽບໃນແບບຈໍາລອງເຫຼົ່ານີ້ແມ່ນມີຄວາມທ້າທາຍເພາະວ່າການສຶກສາເຫຼົ່ານີ້ມີຕົວແປຫຼາຍເກີນໄປ.ຢ່າງໃດກໍຕາມ, ບາງການສຶກສາທາງດ້ານການຊ່ວຍໄດ້ແກ້ໄຂຜົນກະທົບ nociceptive ແລະ analgesic ຂອງ PRP.ການສຶກສາຈໍານວນຫນຶ່ງໄດ້ສະແດງໃຫ້ເຫັນວ່າຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວສໍາລັບ tendinosis ຫຼື rotator cuff tears ມີການບັນເທົາອາການເຈັບປວດເລັກນ້ອຍ.ໃນທາງກົງກັນຂ້າມ, ການສຶກສາອື່ນໆຈໍານວນຫນຶ່ງໄດ້ສະແດງໃຫ້ເຫັນວ່າ PRP ສາມາດຫຼຸດຜ່ອນຫຼືແມ້ກະທັ້ງການລົບລ້າງຄວາມເຈັບປວດຂອງຄົນເຈັບທີ່ມີການເສື່ອມໂຊມຂອງ tendon, OA, plantar fasciitis ແລະພະຍາດຕີນແລະຂໍ້ຕີນອື່ນໆ.ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ສຸດທ້າຍແລະອົງປະກອບຂອງເຊນທາງຊີວະພາບໄດ້ຖືກລະບຸວ່າເປັນຄຸນລັກສະນະ PRP ທີ່ສໍາຄັນ, ເຊິ່ງຊ່ວຍສັງເກດເຫັນຜົນກະທົບຂອງຢາແກ້ປວດທີ່ສອດຄ່ອງຫຼັງຈາກການນໍາໃຊ້ PRP.ຕົວແປອື່ນໆປະກອບມີວິທີການຈັດສົ່ງ PRP, ເຕັກໂນໂລຢີຄໍາຮ້ອງສະຫມັກ, ໂປໂຕຄອນກະຕຸ້ນ platelet, ລະດັບກິດຈະກໍາທາງຊີວະພາບຂອງ PGF ແລະ cytokines ທີ່ຖືກປ່ອຍອອກມາ, ປະເພດຂອງເນື້ອເຍື່ອຂອງຄໍາຮ້ອງສະຫມັກ PRP ແລະປະເພດການບາດເຈັບ.
ມັນເປັນທີ່ຫນ້າສັງເກດທີ່ Kuffler ແກ້ໄຂທ່າແຮງຂອງ PRP ໃນການຫຼຸດຜ່ອນຄວາມເຈັບປວດໃນຄົນເຈັບທີ່ມີຄວາມເຈັບປວດ neuropathic ຊໍາເຮື້ອເລັກນ້ອຍຫາຮ້າຍແຮງ, ຮອງກັບເສັ້ນປະສາດທີ່ບໍ່ແມ່ນການຟື້ນຟູທີ່ເສຍຫາຍ.ຈຸດປະສົງຂອງການສຶກສານີ້ແມ່ນເພື່ອສືບສວນວ່າຄວາມເຈັບປວດ neuropathic ສາມາດຫຼຸດລົງຫຼືຫຼຸດລົງຍ້ອນ PRP ສົ່ງເສີມການຟື້ນຟູ axonal ແລະການ reinnervation ເສັ້ນປະສາດເປົ້າຫມາຍ.ເປັນເລື່ອງແປກທີ່, ໃນບັນດາຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວ, ຄວາມເຈັບປວດ neuropathic ຍັງຖືກລົບລ້າງຫຼືຫຼຸດລົງຢ່າງຫນ້ອຍຫົກປີຫຼັງຈາກການຜ່າຕັດ.ນອກຈາກນັ້ນ, ຄົນເຈັບທັງຫມົດໄດ້ເລີ່ມຕົ້ນທີ່ຈະບັນເທົາອາການເຈັບປວດພາຍໃນສາມອາທິດຫຼັງຈາກການສະຫມັກ PRP.
ບໍ່ດົນມານີ້, ຜົນກະທົບຂອງຢາແກ້ປວດທີ່ຄ້າຍຄືກັນ PRP ໄດ້ຖືກສັງເກດເຫັນໃນຂົງເຂດຂອງບາດແຜຫຼັງການຜ່າຕັດແລະການດູແລຜິວຫນັງ.ຫນ້າສົນໃຈ, ຜູ້ຂຽນໄດ້ລາຍງານລັກສະນະທາງ physiological ຂອງອາການເຈັບປວດບາດແຜທີ່ກ່ຽວຂ້ອງກັບການບາດເຈັບ vascular ແລະ hypoxia ຂອງເນື້ອເຍື່ອຜິວຫນັງ.ພວກເຂົາເຈົ້າຍັງໄດ້ປຶກສາຫາລືກ່ຽວກັບຄວາມສໍາຄັນຂອງ angiogenesis ໃນການເພີ່ມປະສິດທິພາບຂອງອົກຊີເຈນແລະການຈັດສົ່ງທາດອາຫານ.ການສຶກສາຂອງພວກເຂົາໄດ້ສະແດງໃຫ້ເຫັນວ່າການປຽບທຽບກັບກຸ່ມຄວບຄຸມ, ຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວ PRP ມີຄວາມເຈັບປວດຫນ້ອຍແລະ angiogenesis ເພີ່ມຂຶ້ນຢ່າງຫຼວງຫຼາຍ.ສຸດທ້າຍ, Johal ແລະເພື່ອນຮ່ວມງານຂອງລາວໄດ້ດໍາເນີນການທົບທວນລະບົບແລະການວິເຄາະ meta ແລະສະຫຼຸບວ່າ PRP ສາມາດຫຼຸດຜ່ອນຄວາມເຈັບປວດຫຼັງຈາກໃຊ້ PRP ໃນຕົວຊີ້ວັດ orthopedic, ໂດຍສະເພາະໃນຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວໂຣກ epicondylitis ພາຍນອກແລະຫົວເຂົ່າ OA.ແຕ່ຫນ້າເສຍດາຍ, ການສຶກສານີ້ບໍ່ໄດ້ລະບຸຜົນກະທົບຂອງເມັດເລືອດຂາວ, ຄວາມເຂັ້ມຂົ້ນຂອງ platelet ຫຼືການນໍາໃຊ້ຕົວກະຕຸ້ນ platelet exogenous, ເພາະວ່າຕົວແປເຫຼົ່ານີ້ຈະມີຜົນກະທົບຕໍ່ປະສິດທິພາບໂດຍລວມຂອງ PRP.ຄວາມເຂັ້ມຂຸ້ນຂອງ PRP platelet ທີ່ດີທີ່ສຸດສໍາລັບການບັນເທົາອາການເຈັບປວດສູງສຸດແມ່ນບໍ່ຈະແຈ້ງ.ໃນຮູບແບບຫນູຂອງ tendinosis, ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ແມ່ນ 1.0 × 10 6 / μ At L, ຄວາມເຈັບປວດສາມາດບັນເທົາໄດ້ຢ່າງສົມບູນ, ໃນຂະນະທີ່ການບັນເທົາອາການເຈັບປວດທີ່ເກີດຈາກ PRP ກັບເຄິ່ງຫນຶ່ງຂອງຄວາມເຂັ້ມຂົ້ນຂອງ platelet ແມ່ນຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ.ດັ່ງນັ້ນ, ພວກເຮົາຊຸກຍູ້ໃຫ້ມີການສຶກສາທາງດ້ານຄລີນິກຫຼາຍຂຶ້ນເພື່ອສືບສວນຜົນກະທົບຂອງຢາແກ້ປວດຂອງການກະກຽມ PRP ທີ່ແຕກຕ່າງກັນ.
PRP ແລະຜົນກະທົບ angiogenesis
ການກະກຽມ C-PRP ໃນຢາປົວພະຍາດຟື້ນຟູທີ່ຊັດເຈນອະນຸຍາດໃຫ້ສົ່ງ biomolecules ປ່ອຍອອກມາໂດຍຄວາມເຂັ້ມຂຸ້ນສູງຂອງ platelets activated ຢູ່ສະຖານທີ່ເນື້ອເຍື່ອ.ດັ່ງນັ້ນ, ຫຼາຍໆປະຕິກິລິຍາ cascade ໄດ້ຖືກລິເລີ່ມ, ເຊິ່ງປະກອບສ່ວນເຂົ້າໃນການຄວບຄຸມພູມຕ້ານທານ, ຂະບວນການອັກເສບແລະ angiogenesis ເພື່ອສົ່ງເສີມການປິ່ນປົວແລະການສ້ອມແປງເນື້ອເຍື່ອ.
Angiogenesis ແມ່ນຂະບວນການຫຼາຍຂັ້ນຕອນແບບເຄື່ອນໄຫວທີ່ກ່ຽວຂ້ອງກັບການແຕກງອກແລະຈຸລັງ microvessels ຈາກເສັ້ນເລືອດກ່ອນທີ່ມີຢູ່ແລ້ວ.Angiogenesis ມີຄວາມຄືບຫນ້າເນື່ອງຈາກກົນໄກທາງຊີວະພາບທີ່ຫລາກຫລາຍ, ລວມທັງການເຄື່ອນຍ້າຍຂອງເຊນ endothelial, ການຂະຫຍາຍພັນ, ຄວາມແຕກຕ່າງແລະການແບ່ງສ່ວນ.ຂະບວນການ cellular ເຫຼົ່ານີ້ແມ່ນເງື່ອນໄຂເບື້ອງຕົ້ນສໍາລັບການສ້າງຕັ້ງຂອງເສັ້ນເລືອດໃຫມ່.ພວກມັນເປັນສິ່ງຈໍາເປັນສໍາລັບການຂະຫຍາຍຕົວຂອງເສັ້ນເລືອດກ່ອນຫນ້າເພື່ອຟື້ນຟູການໄຫຼວຽນຂອງເລືອດແລະສະຫນັບສະຫນູນກິດຈະກໍາ metabolic ສູງຂອງການສ້ອມແປງເນື້ອເຍື່ອແລະການຟື້ນຟູເນື້ອເຍື່ອ.ເສັ້ນເລືອດໃຫມ່ເຫຼົ່ານີ້ຊ່ວຍໃຫ້ການຈັດສົ່ງອົກຊີເຈນແລະສານອາຫານ, ແລະການໂຍກຍ້າຍຂອງຜະລິດຕະພັນຈາກເນື້ອເຍື່ອທີ່ໄດ້ຮັບການປິ່ນປົວ.
ກິດຈະກໍາ Angiogenesis ຖືກຄວບຄຸມໂດຍການກະຕຸ້ນປັດໄຈ angiogenic VEGF ແລະປັດໃຈຕ້ານ angiogenic (ຕົວຢ່າງ, angiostatin ແລະ thrombospondin-1 [TSP-1]).ໃນສະພາບແວດລ້ອມຈຸນລະພາກທີ່ຕິດເຊື້ອແລະຊຸດໂຊມ (ລວມທັງຄວາມກົດດັນຂອງອົກຊີເຈນຕ່ໍາ, pH ຕ່ໍາແລະລະດັບອາຊິດ lactic ສູງ), ປັດໃຈ angiogenic ທ້ອງຖິ່ນຈະຟື້ນຟູກິດຈະກໍາ angiogenesis.
ສື່ທີ່ລະລາຍຂອງ platelet ຫຼາຍ, ເຊັ່ນ FGF ພື້ນຖານແລະ TGF- βແລະ VEGF ສາມາດກະຕຸ້ນໃຫ້ຈຸລັງ endothelial ຜະລິດເສັ້ນເລືອດໃຫມ່.Landsdown ແລະ Fortier ລາຍງານຜົນໄດ້ຮັບຕ່າງໆທີ່ກ່ຽວຂ້ອງກັບອົງປະກອບ PRP, ລວມທັງແຫຼ່ງ intraplatelet ຂອງ regulators angiogenic ຫຼາຍ.ນອກຈາກນັ້ນ, ພວກເຂົາເຈົ້າໄດ້ສະຫຼຸບວ່າການເພີ່ມຂື້ນຂອງ angiogenesis ປະກອບສ່ວນເຂົ້າໃນການປິ່ນປົວພະຍາດ MSK ໃນເຂດທີ່ມີ vascularization ທີ່ບໍ່ດີ, ເຊັ່ນ: meniscus tear, ການບາດເຈັບຂອງ tendon ແລະພື້ນທີ່ອື່ນໆທີ່ມີ vascularization ທີ່ບໍ່ດີ.
ການສົ່ງເສີມແລະຄຸນສົມບັດຕ້ານການ platelet angiogenic
ໃນສອງສາມທົດສະວັດທີ່ຜ່ານມາ, ການສຶກສາທີ່ຈັດພີມມາໄດ້ພິສູດວ່າ platelets ມີບົດບາດສໍາຄັນໃນ hemostasis ປະຖົມ, ການສ້າງກ້ອນຫີນ, ປັດໄຈການຂະຫຍາຍຕົວແລະການປ່ອຍ cytokine, ແລະລະບຽບການ angiogenesis ເປັນສ່ວນຫນຶ່ງຂອງຂະບວນການສ້ອມແປງເນື້ອເຍື່ອ.Paradoxically, PRP α- granules ປະກອບດ້ວຍສານຫນູຂອງປັດໄຈການຂະຫຍາຍຕົວ pro-angiogenic, ທາດໂປຼຕີນຈາກຕ້ານ angiogenic ແລະ cytokines (ເຊັ່ນ: PF4, plasminogen activator inhibitor-1 ແລະ TSP-1), ແລະເປົ້າຫມາຍການປ່ອຍຂອງປັດໃຈສະເພາະທີ່ມີບົດບາດ. .ພາລະບົດບາດໃນ angiogenesis.ດັ່ງນັ້ນ, ບົດບາດຂອງ PRP ໃນການຄວບຄຸມລະບຽບການ angiogenesis ອາດຈະຖືກກໍານົດໂດຍການກະຕຸ້ນຂອງ receptors ພື້ນຜິວຂອງເຊນສະເພາະ, TGF- β Initiate pro-angiogenic ແລະປະຕິກິລິຍາຕ້ານ angiogenic.ຄວາມສາມາດຂອງ platelets ໃນການປະຕິບັດເສັ້ນທາງ angiogenesis ໄດ້ຖືກຢືນຢັນໃນ pathological angiogenesis ແລະ tumor angiogenesis.
Platelet-derived ປັດໄຈການຂະຫຍາຍຕົວ angiogenic ແລະປັດໄຈການຂະຫຍາຍຕົວຕ້ານ angiogenic, ໄດ້ມາຈາກ α- ແລະໂມເລກຸນທີ່ຫນາແຫນ້ນແລະກາວ.ສິ່ງທີ່ ສຳ ຄັນທີ່ສຸດ, ມັນໄດ້ຖືກຍອມຮັບໂດຍທົ່ວໄປວ່າຜົນກະທົບໂດຍລວມຂອງ platelets ກ່ຽວກັບ angiogenesis ແມ່ນ pro-angiogenic ແລະກະຕຸ້ນ.ມັນຄາດວ່າການປິ່ນປົວດ້ວຍ PRP ຈະຄວບຄຸມ induction ຂອງ angiogenesis, ເຊິ່ງຈະປະກອບສ່ວນເຂົ້າໃນການປິ່ນປົວຜົນກະທົບຂອງພະຍາດຈໍານວນຫຼາຍ, ເຊັ່ນ: ການປິ່ນປົວບາດແຜແລະການສ້ອມແປງເນື້ອເຍື່ອ.ການບໍລິຫານຂອງ PRP, ໂດຍສະເພາະການບໍລິຫານຂອງ PGF ຄວາມເຂັ້ມຂົ້ນສູງແລະ cytokines platelet ອື່ນໆ, ສາມາດ induce angiogenesis, angiogenesis ແລະ arteriogenesis, ເນື່ອງຈາກວ່າ stromal cell-derived factor 1a ຜູກມັດກັບ receptor CXCR4 ໃນຈຸລັງ progenitor endothelial.Bill et al.ມັນໄດ້ຖືກແນະນໍາວ່າ PRP ເພີ່ມ ischemic neovascularization, ເຊິ່ງອາດຈະເປັນຍ້ອນການກະຕຸ້ນຂອງ angiogenesis, angiogenesis ແລະ arteriogenesis.ໃນຮູບແບບ in vitro ຂອງເຂົາເຈົ້າ, ການຂະຫຍາຍຈຸລັງ endothelial ແລະການສ້າງ capillary ໄດ້ຖືກກະຕຸ້ນໂດຍ PDGs ທີ່ແຕກຕ່າງກັນຈໍານວນຫລາຍ, ຊຶ່ງໃນນັ້ນ VEGF ແມ່ນຕົວກະຕຸ້ນ angiogenic ຕົ້ນຕໍ.ປັດໄຈທີ່ສໍາຄັນແລະສໍາຄັນອີກອັນຫນຶ່ງສໍາລັບການຟື້ນຟູເສັ້ນທາງ angiogenesis ແມ່ນການປະສົມປະສານລະຫວ່າງ PGFs ຫຼາຍ.Richardson et al.ມັນໄດ້ຖືກພິສູດວ່າກິດຈະກໍາ synergistic ຂອງປັດໄຈ angiogenic platelet-derived growth factor-bb (PDGF-BB) ແລະ VEGF ນໍາໄປສູ່ການສ້າງຕັ້ງຢ່າງໄວວາຂອງເຄືອຂ່າຍ vascular mature ເມື່ອທຽບກັບກິດຈະກໍາຂອງປັດໄຈການຂະຫຍາຍຕົວຂອງບຸກຄົນ.ຜົນກະທົບລວມຂອງປັດໃຈເຫຼົ່ານີ້ໄດ້ຖືກຢືນຢັນເມື່ອໄວໆມານີ້ໃນການສຶກສາກ່ຽວກັບການປັບປຸງການໄຫຼວຽນຂອງສະຫມອງໃນຫນູທີ່ມີ hypoperfusion ໃນໄລຍະຍາວ.
ສິ່ງທີ່ ສຳ ຄັນທີ່ສຸດ, ການສຶກສາໃນ vitro ໄດ້ວັດແທກຜົນກະທົບຂອງການແຜ່ຂະຫຍາຍຂອງຈຸລັງ endothelial ກ່າງໃບ ໜ້າ ຂອງມະນຸດແລະຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ຕ່າງໆໃນການເລືອກອຸປະກອນການກະກຽມ PRP ແລະຍຸດທະສາດປະລິມານ platelet, ແລະຜົນໄດ້ຮັບສະແດງໃຫ້ເຫັນວ່າປະລິມານ platelet ທີ່ດີທີ່ສຸດແມ່ນ 1.5 × 10 6 platelets / μ. 50. ເພື່ອສົ່ງເສີມ angiogenesis.ຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ສູງເກີນໄປອາດຈະຂັດຂວາງຂະບວນການ angiogenesis, ດັ່ງນັ້ນຜົນກະທົບແມ່ນບໍ່ດີ.
Cell aging, aging ແລະ PRP
ເຊລເຊລສາມາດຖືກກະຕຸ້ນໂດຍການກະຕຸ້ນຕ່າງໆ.ນີ້ແມ່ນຂະບວນການທີ່ຈຸລັງຢຸດເຊົາການແບ່ງແລະຜ່ານການປ່ຽນແປງ phenotypic ເປັນເອກະລັກເພື່ອປ້ອງກັນການຂະຫຍາຍຕົວທີ່ບໍ່ຈໍາກັດຂອງຈຸລັງທີ່ຖືກທໍາລາຍ, ເຊິ່ງມີບົດບາດສໍາຄັນໃນການປ້ອງກັນມະເຮັງ.ໃນຂະບວນການຂອງ physiological aging, aging replication ຂອງເຊນຍັງຈະສົ່ງເສີມການ aging ຂອງເຊນ, ແລະຄວາມສາມາດໃນການຟື້ນຟູຂອງ MSCs ຈະຫຼຸດລົງ.
ຜົນກະທົບຂອງການແກ່ໄວແລະໄວຂອງເຊນ
ໃນ vivo, ຈຸລັງຫຼາຍຊະນິດຈະມີອາຍຸແລະສະສົມຢູ່ໃນເນື້ອເຍື່ອຕ່າງໆໃນເວລາຜູ້ສູງອາຍຸ, ໃນນັ້ນມີຈໍານວນຈຸລັງທີ່ມີອາຍຸຫຼາຍ.ການສະສົມຂອງຈຸລັງຜູ້ສູງອາຍຸເບິ່ງຄືວ່າຈະເພີ່ມຂຶ້ນກັບການເພີ່ມຂຶ້ນຂອງອາຍຸ, ຄວາມເສຍຫາຍຂອງລະບົບພູມຕ້ານທານ, ຄວາມເສຍຫາຍຂອງເນື້ອເຍື່ອຫຼືປັດໃຈທີ່ກ່ຽວຂ້ອງກັບຄວາມກົດດັນ.ກົນໄກຂອງຄວາມສູງອາຍຸຂອງເຊນໄດ້ຖືກກໍານົດວ່າເປັນປັດໄຈທີ່ເຮັດໃຫ້ເກີດພະຍາດຂອງພະຍາດທີ່ກ່ຽວຂ້ອງກັບອາຍຸເຊັ່ນ: ໂລກຂໍ້ອັກເສບ, ໂລກກະດູກພຸນແລະການ degeneration ຂອງແຜ່ນດິດ intervertebral.ຄວາມຫຼາກຫຼາຍຂອງສິ່ງກະຕຸ້ນຈະເຮັດໃຫ້ເຊວເຊລຍິ່ງຮ້າຍແຮງຂຶ້ນ.ໃນການຕອບສະຫນອງ, phenotype secretory ທີ່ກ່ຽວຂ້ອງກັບ senescence (SASP) ຈະ secrete ຄວາມເຂັ້ມຂຸ້ນສູງຂອງຈຸລັງທາດໂປຼຕີນແລະ cytokines.phenotype ພິເສດນີ້ແມ່ນກ່ຽວຂ້ອງກັບຈຸລັງຜູ້ສູງອາຍຸ, ເຊິ່ງພວກມັນ secrete ລະດັບສູງຂອງ cytokines ອັກເສບ (ເຊັ່ນ IL-1, IL-6, IL-8), ປັດໃຈການຂະຫຍາຍຕົວ (ເຊັ່ນ: TGF- β, HGF, VEGF, PDGF), MMP, ແລະ cathepsin.ເມື່ອປຽບທຽບກັບຄົນຫນຸ່ມສາວ, SAPS ໄດ້ຖືກພິສູດວ່າເພີ່ມຂຶ້ນຕາມອາຍຸ, ເພາະວ່າຂະບວນການຄົງທີ່ຂອງສະພາບໄດ້ຖືກທໍາລາຍ, ເຮັດໃຫ້ເກີດຄວາມແກ່ຂອງເຊນແລະຄວາມສາມາດໃນການຟື້ນຟູທີ່ຫຼຸດລົງ.ໂດຍສະເພາະ, ໃນພະຍາດຮ່ວມກັນແລະພະຍາດກ້າມຊີ້ນ skeletal.ໃນເລື່ອງນີ້, ຄວາມສູງຂອງພູມຕ້ານທານແມ່ນຖືວ່າເປັນການປ່ຽນແປງທີ່ສໍາຄັນໃນຄວາມລັບຂອງຈຸລັງພູມຕ້ານທານ, ເຊິ່ງຊີ້ໃຫ້ເຫັນວ່າຄວາມເຂັ້ມຂົ້ນຂອງ TNF-a, IL-6 ແລະ / ຫຼື Il-1b ເພີ່ມຂຶ້ນ, ນໍາໄປສູ່ການອັກເສບຊໍາເຮື້ອໃນລະດັບຕ່ໍາ.ມັນເປັນມູນຄ່າທີ່ສັງເກດວ່າ dysfunction ຂອງເຊນລໍາຕົ້ນຍັງກ່ຽວຂ້ອງກັບກົນໄກການອັດຕະໂນມັດທີ່ບໍ່ແມ່ນເຊນ, ເຊັ່ນ: ຈຸລັງຜູ້ສູງອາຍຸ, ໂດຍສະເພາະແມ່ນການຜະລິດຂອງປັດໃຈຕ້ານການອັກເສບແລະຕ້ານການເກີດໃຫມ່ໂດຍຜ່ານ SASP.
ໃນທາງກົງກັນຂ້າມ, SASP ຍັງສາມາດກະຕຸ້ນຄວາມສຕິກຂອງເຊນ ແລະການສ້າງເຊລທີ່ຕິດກັນຄືນໃໝ່.ນອກຈາກນັ້ນ, SASP ສາມາດຈັດຕັ້ງການສື່ສານກັບຜູ້ໄກ່ເກ່ຍພູມຕ້ານທານຕ່າງໆແລະກະຕຸ້ນຈຸລັງພູມຕ້ານທານເພື່ອສົ່ງເສີມການລ້າງຈຸລັງຜູ້ສູງອາຍຸ.ຄວາມເຂົ້າໃຈກ່ຽວກັບບົດບາດແລະຫນ້າທີ່ຂອງຈຸລັງຜູ້ສູງອາຍຸຈະປະກອບສ່ວນເຂົ້າໃນການປິ່ນປົວແລະການຟື້ນຟູເນື້ອເຍື່ອຂອງກ້າມຊີ້ນ MSK ແລະບາດແຜຊໍາເຮື້ອ.
ມັນເປັນທີ່ສັງເກດວ່າ Ritcka et al.ການສຶກສາຢ່າງກວ້າງຂວາງໄດ້ຖືກປະຕິບັດ, ແລະບົດບາດຕົ້ນຕໍແລະເປັນປະໂຫຍດຂອງ SASP ໃນການສົ່ງເສີມການສຕິກຂອງເຊນແລະການຟື້ນຟູເນື້ອເຍື່ອໄດ້ຖືກຄົ້ນພົບ, ແລະແນວຄວາມຄິດຂອງການປິ່ນປົວແບບຊົ່ວຄາວຂອງຈຸລັງຜູ້ສູງອາຍຸໄດ້ຖືກນໍາສະເຫນີ.ພວກເຂົາເຈົ້າໄດ້ກ່າວຢ່າງລະມັດລະວັງວ່າການແກ່ຍາວສ່ວນໃຫຍ່ແມ່ນເປັນຂະບວນການທີ່ເປັນປະໂຫຍດແລະການຟື້ນຟູ.
ການແກ່ອາຍຸຂອງເຊນແລະທ່າແຮງຂອງ PRP
ເມື່ອຈໍານວນຂອງຈຸລັງລໍາຕົ້ນຫຼຸດລົງ, ອາຍຸຈະສົ່ງຜົນກະທົບຕໍ່ການປະຕິບັດຂອງຈຸລັງລໍາຕົ້ນ.ເຊັ່ນດຽວກັນ, ໃນມະນຸດ, ລັກສະນະຂອງເຊນລໍາຕົ້ນ (ເຊັ່ນ: ຄວາມແຫ້ງແລ້ງ, ການຂະຫຍາຍໂຕ ແລະຄວາມແຕກຕ່າງ) ຍັງຫຼຸດລົງຕາມອາຍຸ.Wang ແລະ Nirmala ລາຍງານວ່າຜູ້ສູງອາຍຸຈະຫຼຸດຜ່ອນຄຸນລັກສະນະຂອງຈຸລັງລໍາຕົ້ນຂອງຈຸລັງ tendon ແລະຈໍານວນຂອງ receptors ປັດໄຈການຂະຫຍາຍຕົວ.ການສຶກສາສັດໄດ້ສະແດງໃຫ້ເຫັນວ່າຄວາມເຂັ້ມຂົ້ນຂອງ PDGF ໃນມ້າຫນຸ່ມແມ່ນສູງ.ພວກເຂົາເຈົ້າໄດ້ສະຫຼຸບວ່າການເພີ່ມຂຶ້ນຂອງຈໍານວນຂອງ GF receptors ແລະຈໍານວນຂອງ GF ໃນບຸກຄົນໄວຫນຸ່ມອາດຈະໄດ້ຮັບການຕອບສະຫນອງ cellular ທີ່ດີກວ່າການປິ່ນປົວ PRP ຫຼາຍກ່ວາຜູ້ສູງອາຍຸໃນບຸກຄົນໄວຫນຸ່ມ.ການຄົ້ນພົບເຫຼົ່ານີ້ເປີດເຜີຍວ່າເປັນຫຍັງການປິ່ນປົວ PRP ອາດຈະມີປະສິດທິພາບຫນ້ອຍຫຼືແມ້ກະທັ້ງບໍ່ມີປະສິດຕິຜົນໃນຄົນເຈັບຜູ້ສູງອາຍຸທີ່ມີຈຸລັງລໍາຕົ້ນຫນ້ອຍແລະ "ຄຸນນະພາບທີ່ບໍ່ດີ".ມັນໄດ້ຖືກພິສູດວ່າຂະບວນການອາຍຸຂອງ cartilage ແກ່ແມ່ນປີ້ນກັບກັນແລະໄລຍະເວລາພັກຜ່ອນຂອງ chondrocytes ແມ່ນເພີ່ມຂຶ້ນຫຼັງຈາກການສັກຢາ PRP.Jia et al.ມັນຖືກນໍາໃຊ້ເພື່ອສຶກສາ fibroblasts dermal ຫນູໃນການຖ່າຍຮູບ vitro, ມີແລະບໍ່ມີການປິ່ນປົວ PRP, ເພື່ອຊີ້ແຈງກົນໄກຂອງ counteraction PGF ໃນຮູບແບບນີ້.ກຸ່ມ PRP ສະແດງໃຫ້ເຫັນຜົນກະທົບໂດຍກົງຕໍ່ extracellular matrix, ເພີ່ມ collagen ປະເພດ I ແລະຫຼຸດລົງການສັງເຄາະຂອງ metalloproteinases, ຊີ້ໃຫ້ເຫັນວ່າ PRP ສາມາດຕ້ານການ aging ຂອງເຊນ, ແລະຍັງຢູ່ໃນພະຍາດ MSK degenerative.
ໃນການສຶກສາອື່ນ, PRP ໄດ້ຖືກນໍາໃຊ້ເພື່ອເກັບກໍາຈຸລັງໄຂກະດູກອາຍຸຈາກຫນູທີ່ມີອາຍຸ.ມັນໄດ້ຖືກກໍານົດວ່າ PRP ສາມາດຟື້ນຟູຄວາມຫລາກຫລາຍຂອງການເຮັດວຽກຂອງເຊນລໍາຕົ້ນຈາກການແກ່, ເຊັ່ນ: ການຂະຫຍາຍຈຸລັງແລະການສ້າງຕັ້ງອານານິຄົມ, ແລະສ້າງເຄື່ອງຫມາຍທີ່ກ່ຽວຂ້ອງກັບອາຍຸຂອງເຊນຄືນໃຫມ່.
ບໍ່ດົນມານີ້, Oberlohr ແລະເພື່ອນຮ່ວມງານຂອງລາວໄດ້ສຶກສາຢ່າງກວ້າງຂວາງກ່ຽວກັບບົດບາດຂອງ cell aging ໃນການຟື້ນຟູກ້າມຊີ້ນທີ່ອ່ອນເພຍ, ແລະປະເມີນ PRP ແລະ platelet-poor plasma (PPP) ເປັນທາງເລືອກການປິ່ນປົວທາງຊີວະພາບສໍາລັບການສ້ອມແປງກ້າມຊີ້ນ skeletal.ພວກເຂົາເຈົ້າໄດ້ຈິນຕະນາການວ່າການປິ່ນປົວ PRP ຫຼື PPP ສໍາລັບການສ້ອມແປງກ້າມຊີ້ນກະດູກສັນຫຼັງແມ່ນອີງໃສ່ປັດໃຈທາງຊີວະພາບທີ່ກໍາຫນົດເອງສໍາລັບເຄື່ອງຫມາຍເຊນສະເພາະ SASP ແລະປັດໃຈອື່ນໆທີ່ນໍາໄປສູ່ການພັດທະນາ fibrosis.
ມັນສົມເຫດສົມຜົນທີ່ຈະເຊື່ອວ່າກ່ອນທີ່ຈະນໍາໃຊ້ PRP, ອາຍຸຂອງເຊນທີ່ຖືກເປົ້າຫມາຍສາມາດປັບປຸງລັກສະນະການຟື້ນຟູຂອງປະສິດທິພາບການປິ່ນປົວທາງຊີວະພາບໂດຍການຫຼຸດຜ່ອນປັດໃຈ SASP ທ້ອງຖິ່ນ.ມັນໄດ້ຖືກແນະນໍາວ່າທາງເລືອກອື່ນໃນການປັບປຸງຜົນໄດ້ຮັບຂອງການປິ່ນປົວ PRP ແລະ PPP ສໍາລັບການຟື້ນຟູກ້າມຊີ້ນ skeletal ແມ່ນການເລືອກເອົາຈຸລັງຜູ້ສູງອາຍຸດ້ວຍ scavengers aging.ບໍ່ມີຄວາມສົງໃສວ່າຜົນການຄົ້ນຄວ້າທີ່ຜ່ານມາກ່ຽວກັບຜົນກະທົບຂອງ PRP ຕໍ່ການຈະເລີນເຕີບໂຕຂອງເຊນແລະຄວາມສູງອາຍຸແມ່ນຫນ້າສົນໃຈ, ແຕ່ພວກເຂົາຍັງຢູ່ໃນຂັ້ນຕອນເບື້ອງຕົ້ນ.ດັ່ງນັ້ນ, ມັນບໍ່ສົມເຫດສົມຜົນທີ່ຈະໃຫ້ຄໍາແນະນໍາໃດໆໃນເວລານີ້.
(ເນື້ອໃນຂອງບົດຄວາມນີ້ຖືກພິມຄືນ, ແລະພວກເຮົາບໍ່ໄດ້ສະຫນອງການຮັບປະກັນຄວາມຖືກຕ້ອງ, ຄວາມຫນ້າເຊື່ອຖືຫຼືຄວາມສົມບູນຂອງເນື້ອໃນທີ່ມີຢູ່ໃນບົດຄວາມນີ້, ແລະບໍ່ຮັບຜິດຊອບຕໍ່ຄວາມຄິດເຫັນຂອງບົດຄວາມນີ້, ກະລຸນາເຂົ້າໃຈ.)
ເວລາປະກາດ: ວັນທີ 01-01-2023