ໃນມື້ນີ້, ແນວຄວາມຄິດທີ່ເອີ້ນວ່າ PRP ໄດ້ປະກົດຕົວຄັ້ງທໍາອິດໃນພາກສະຫນາມຂອງ hematology ໃນຊຸມປີ 1970.ນັກວິທະຍາສາດດ້ານເລືອດສ້າງຄໍາສັບ PRP ເມື່ອທົດສະວັດກ່ອນຫນ້ານີ້ເພື່ອອະທິບາຍ plasma ທີ່ໄດ້ຮັບຈາກການນັບ platelet ສູງກວ່າມູນຄ່າພື້ນຖານຂອງເລືອດ peripheral.ຫຼາຍກວ່າສິບປີຕໍ່ມາ, PRP ໄດ້ຖືກນໍາໃຊ້ໃນການຜ່າຕັດ maxillofacial ເປັນຮູບແບບຂອງ platelet ອຸດົມສົມບູນ fibrin (PRF).ເນື້ອໃນຂອງ fibrin ໃນອະນຸພັນ PRP ນີ້ມີມູນຄ່າທີ່ສໍາຄັນເນື່ອງຈາກຄວາມຫນຽວແລະລັກສະນະສະຫມໍ່າສະເຫມີ, ໃນຂະນະທີ່ PRP ມີຄຸນສົມບັດຕ້ານການອັກເສບແບບຍືນຍົງແລະກະຕຸ້ນການຂະຫຍາຍຈຸລັງ.ໃນທີ່ສຸດ, ປະມານຊຸມປີ 1990, PRP ເລີ່ມກາຍເປັນທີ່ນິຍົມ.ສຸດທ້າຍ, ເຕັກໂນໂລຢີນີ້ໄດ້ຖືກໂອນໄປຫາຂົງເຂດທາງການແພດອື່ນໆ.ນັບຕັ້ງແຕ່ນັ້ນມາ, ຊີວະວິທະຍາໃນທາງບວກນີ້ໄດ້ຖືກສຶກສາຢ່າງກວ້າງຂວາງແລະນໍາໃຊ້ກັບການປິ່ນປົວການບາດເຈັບຂອງກ້າມຊີ້ນຕ່າງໆຂອງນັກກິລາມືອາຊີບ, ເຊິ່ງໄດ້ສົ່ງເສີມຄວາມສົນໃຈຢ່າງກວ້າງຂວາງໃນສື່ມວນຊົນ.ນອກເຫນືອໄປຈາກປະສິດທິພາບໃນ orthopedics ແລະຢາກິລາ, PRP ຍັງຖືກນໍາໃຊ້ໃນ ophthalmology, gynecology, urology ແລະ cardiology, pediatrics ແລະການຜ່າຕັດສຕິກ.ໃນຊຸມປີມໍ່ໆມານີ້, PRP ຍັງໄດ້ຮັບການຍ້ອງຍໍຈາກແພດຜິວຫນັງສໍາລັບທ່າແຮງໃນການປິ່ນປົວບາດແຜຜິວຫນັງ, ການສ້ອມແປງຮອຍແປ້ວ, ການຟື້ນຟູເນື້ອເຍື່ອ, ການຟື້ນຟູຜິວຫນັງແລະແມ້ກະທັ້ງການສູນເສຍຜົມ.
ພິຈາລະນາຄວາມຈິງທີ່ວ່າ PRP ສາມາດແກ້ໄຂໂດຍກົງໃນຂະບວນການປິ່ນປົວແລະການອັກເສບ, ມັນເປັນສິ່ງຈໍາເປັນທີ່ຈະແນະນໍາ cascade ການປິ່ນປົວເປັນເອກະສານອ້າງອີງ.ຂະບວນການປິ່ນປົວໄດ້ຖືກແບ່ງອອກເປັນສີ່ຂັ້ນຕອນດັ່ງຕໍ່ໄປນີ້: hemostasis;ການອັກເສບ;ການຂະຫຍາຍຈຸລັງ ແລະມາຕຣິກເບື້ອງ, ແລະສຸດທ້າຍແມ່ນການສ້າງບາດແຜ.
ການປິ່ນປົວເນື້ອເຍື່ອ
ຕິກິຣິຍາ cascade ການປິ່ນປົວເນື້ອເຍື່ອແມ່ນ activated, ເຊິ່ງນໍາໄປສູ່ການສະສົມ platelet ການສ້າງຕັ້ງຂອງ clots ແລະການພັດທະນາຂອງ extracellular matrix ຊົ່ວຄາວ (ECM).ຫຼັງຈາກນັ້ນ, platelets ຕິດກັບ collagen ແລະທາດໂປຼຕີນຈາກ ECM, ກະຕຸ້ນການປ່ອຍໂມເລກຸນທີ່ມີການເຄື່ອນໄຫວທາງຊີວະພາບທີ່ມີຢູ່ໃນ a-granules.Platelets ປະກອບດ້ວຍຫຼາຍໆໂມເລກຸນທາງຊີວະພາບ, ລວມທັງປັດໃຈການຂະຫຍາຍຕົວ, ປັດໃຈການປິ່ນປົວດ້ວຍທາງເຄມີແລະ cytokines, ເຊັ່ນດຽວກັນກັບຕົວໄກ່ເກ່ຍ proinflammatory, ເຊັ່ນ prostaglandin, prostate cyclin, histamine, thromboxane, serotonin ແລະ bradykinin.
ຂັ້ນຕອນສຸດທ້າຍຂອງຂະບວນການປິ່ນປົວແມ່ນຂຶ້ນກັບການແກ້ໄຂບາດແຜ.ການແກ້ໄຂເນື້ອເຍື່ອຖືກຄວບຄຸມຢ່າງເຂັ້ມງວດເພື່ອສ້າງຄວາມສົມດຸນລະຫວ່າງປະຕິກິລິຍາ anabolic ແລະ catabolic.ໃນຂັ້ນຕອນນີ້, ປັດໄຈການເຕີບໂຕຂອງ platelet-derived (PDGF) ແລະການຫັນປ່ຽນປັດໄຈການຂະຫຍາຍຕົວ (TGF- β) Fibronectin ແລະ fibronectin ກະຕຸ້ນການຂະຫຍາຍແລະການເຄື່ອນຍ້າຍຂອງ fibroblasts, ເຊັ່ນດຽວກັນກັບການສັງເຄາະອົງປະກອບ ECM.ຢ່າງໃດກໍ່ຕາມ, ເວລາຂອງການເຕີບໃຫຍ່ຂອງບາດແຜແມ່ນຂຶ້ນກັບລະດັບຄວາມຮ້າຍແຮງຂອງບາດແຜ, ຄຸນລັກສະນະສ່ວນບຸກຄົນແລະຄວາມສາມາດໃນການປິ່ນປົວສະເພາະຂອງເນື້ອເຍື່ອທີ່ບາດເຈັບ.ບາງປັດໃຈທາງໂພຊະນາການແລະການເຜົາຜະຫລານອາຫານສາມາດສົ່ງຜົນກະທົບຕໍ່ຂະບວນການປິ່ນປົວ, ເຊັ່ນ: ເນື້ອເຍື່ອ ischemia, hypoxia, ການຕິດເຊື້ອ, ຄວາມບໍ່ສົມດຸນຂອງປັດໃຈການຂະຫຍາຍຕົວ, ແລະແມ້ກະທັ້ງພະຍາດທີ່ກ່ຽວຂ້ອງກັບໂຣກ metabolic.
ສະພາບແວດລ້ອມຈຸນລະພາກ proinflammatory ແຊກແຊງຂະບວນການປິ່ນປົວ.ຄວາມສັບສົນຫຼາຍແມ່ນວ່າກິດຈະກໍາ protease ສູງ inhibits ການປະຕິບັດທໍາມະຊາດຂອງປັດໄຈການຂະຫຍາຍຕົວ (GF).ນອກເຫນືອໄປຈາກຄຸນສົມບັດ mitotic, angiogenic ແລະ chemotactic ຂອງມັນ, PRP ຍັງເປັນແຫຼ່ງທີ່ອຸດົມສົມບູນຂອງປັດໃຈການຂະຫຍາຍຕົວຫຼາຍ.ຊີວະໂມເລກຸນເຫຼົ່ານີ້ອາດຈະຕ້ານຜົນກະທົບທີ່ເປັນອັນຕະລາຍໃນເນື້ອເຍື່ອອັກເສບໂດຍການຄວບຄຸມການອັກເສບທີ່ເພີ່ມຂຶ້ນແລະການສ້າງຕັ້ງການກະຕຸ້ນ anabolic.ພິຈາລະນາລັກສະນະເຫຼົ່ານີ້, ນັກຄົ້ນຄວ້າອາດຈະຊອກຫາທ່າແຮງອັນໃຫຍ່ຫຼວງໃນການປິ່ນປົວການບາດເຈັບທີ່ສັບສົນຕ່າງໆ.
ພະຍາດຈໍານວນຫຼາຍ, ໂດຍສະເພາະແມ່ນລັກສະນະຂອງ musculoskeletal, ຢ່າງແຂງແຮງແມ່ນຂຶ້ນກັບຜະລິດຕະພັນຊີວະພາບທີ່ຄວບຄຸມຂະບວນການອັກເສບ, ເຊັ່ນ PRP ສໍາລັບການປິ່ນປົວຂອງ osteoarthritis.ໃນກໍລະນີນີ້, ສຸຂະພາບຂອງ cartilage articular ແມ່ນຂຶ້ນກັບຄວາມສົມດູນທີ່ຊັດເຈນຂອງປະຕິກິລິຍາ anabolic ແລະ catabolic.ດ້ວຍຫຼັກການນີ້ຢູ່ໃນໃຈ, ການນໍາໃຊ້ຕົວແທນທາງຊີວະພາບໃນທາງບວກບາງຢ່າງອາດຈະພິສູດຜົນສໍາເລັດໃນການບັນລຸຄວາມສົມດູນທີ່ມີສຸຂະພາບດີ.PRP ເນື່ອງຈາກວ່າມັນປ່ອຍ platelets α- ປັດໄຈການຂະຫຍາຍຕົວທີ່ມີຢູ່ໃນ granules ຖືກນໍາໃຊ້ຢ່າງກວ້າງຂວາງເພື່ອຄວບຄຸມທ່າແຮງຂອງການປ່ຽນເນື້ອເຍື່ອ, ເຊິ່ງຍັງຊ່ວຍຫຼຸດຜ່ອນຄວາມເຈັບປວດ.ໃນຄວາມເປັນຈິງ, ຫນຶ່ງໃນເປົ້າຫມາຍຕົ້ນຕໍຂອງການປິ່ນປົວ PRP ແມ່ນເພື່ອຢຸດການອັກເສບແລະ microenvironment catabolic ຕົ້ນຕໍແລະສົ່ງເສີມການຫັນເປັນຢາຕ້ານການອັກເສບ.ຜູ້ຂຽນອື່ນໆໄດ້ສະແດງໃຫ້ເຫັນກ່ອນຫນ້ານີ້ວ່າ thrombin activated PRP ເພີ່ມການປ່ອຍໂມເລກຸນຊີວະພາບຫຼາຍ.ປັດໃຈເຫຼົ່ານີ້ລວມມີປັດໄຈການຂະຫຍາຍຕົວຂອງ hepatocyte (HGF) ແລະປັດໄຈການຈະເລີນເຕີບໂຕຂອງເນື້ອງອກ (TNF- α), ປັດໄຈການຂະຫຍາຍຕົວຂອງການຂະຫຍາຍຕົວ beta1 (TGF- β 1), vascular endothelial growth factor (VEGF) ແລະ epidermis Growth factor (EGF).ການສຶກສາອື່ນໆໄດ້ສະແດງໃຫ້ເຫັນວ່າ PRP ສົ່ງເສີມການເພີ່ມຂື້ນຂອງປະເພດ ii collagen ແລະລະດັບ mRNA aggrecan, ໃນຂະນະທີ່ຫຼຸດຜ່ອນການຍັບຍັ້ງຂອງ pro-inflammatory cytokine interleukin - (IL) 1 ກ່ຽວກັບພວກມັນ.ມັນຍັງໄດ້ຖືກແນະນໍາວ່າເນື່ອງຈາກ HGF ແລະ TNF- α [28] PRP ອາດຈະຊ່ວຍສ້າງຜົນກະທົບຕ້ານການອັກເສບ.ທັງສອງການກະກຽມໂມເລກຸນເຫຼົ່ານີ້ຫຼຸດຜ່ອນປັດໄຈນິວເຄລຍ kappaB (NF- κВ) ກິດຈະກໍາຕ້ານການກະຕຸ້ນແລະການສະແດງອອກ;ອັນທີສອງ, ໂດຍຜ່ານການສະແດງອອກ TGF- β 1 ຍັງປ້ອງກັນບໍ່ໃຫ້ monocyte chemotaxis, ດັ່ງນັ້ນຈຶ່ງຕ້ານກັບ TNF- αຜົນກະທົບ transactivation ຂອງ chemokines.HGF ເບິ່ງຄືວ່າມີບົດບາດທີ່ຂາດບໍ່ໄດ້ໃນຜົນກະທົບຕ້ານການອັກເສບທີ່ກະຕຸ້ນໂດຍ PRP.cytokine ຕ້ານການອັກເສບທີ່ມີທ່າແຮງນີ້ທໍາລາຍເສັ້ນທາງສັນຍານ NF- κ B ແລະການສະແດງອອກຂອງ cytokine proinflammatory inhibit ການຕອບສະຫນອງອັກເສບ.ນອກຈາກນັ້ນ, PRP ຍັງສາມາດຫຼຸດຜ່ອນລະດັບສູງຂອງ nitric oxide (NO).ສໍາລັບຕົວຢ່າງ, ໃນ cartilage articular, ການເພີ່ມຂື້ນຂອງຄວາມເຂັ້ມຂົ້ນຂອງ NO ໄດ້ຖືກພິສູດເພື່ອຍັບຍັ້ງການສັງເຄາະ collagen ແລະກະຕຸ້ນ chondrocyte apoptosis, ໃນຂະນະທີ່ເພີ່ມການສັງເຄາະຂອງ matrix metalloproteinases (MMPs), ດັ່ງນັ້ນການສົ່ງເສີມການຫັນປ່ຽນ catabolism.ໃນແງ່ຂອງການເສື່ອມສະພາບຂອງເຊນ, PRP ຍັງຖືກພິຈາລະນາວ່າສາມາດຈັດການ autophagy ຂອງປະເພດເຊນສະເພາະ.ເມື່ອເຖິງສະຖານະຜູ້ສູງອາຍຸສຸດທ້າຍ, ບາງກຸ່ມຈຸລັງສູນເສຍທ່າແຮງຂອງສະຖານະຄົງທີ່ແລະການຕໍ່ອາຍຸຕົນເອງ.ຢ່າງໃດກໍ່ຕາມ, ການສຶກສາທີ່ຜ່ານມາໄດ້ສະແດງໃຫ້ເຫັນວ່າການປິ່ນປົວ PRP ສາມາດແກ້ໄຂສະພາບທີ່ເປັນອັນຕະລາຍເຫຼົ່ານີ້ໄດ້ດີ.Moussa ແລະເພື່ອນຮ່ວມງານໄດ້ພິສູດວ່າ PRP ສາມາດກະຕຸ້ນການປົກປ້ອງ chondrocytes ໂດຍການເພີ່ມເຄື່ອງຫມາຍ autophagy ແລະຕ້ານການອັກເສບ, ໃນຂະນະທີ່ການຫຼຸດຜ່ອນ apoptosis ຂອງ cartilage osteoarthritis ຂອງມະນຸດ.Garcia Pratt et al.ມັນໄດ້ຖືກລາຍງານວ່າ autophagy ກໍານົດການປ່ຽນແປງລະຫວ່າງຊະຕາກໍາການພັກຜ່ອນແລະຄວາມສູງອາຍຸຂອງຈຸລັງກ້າມກ້າມ.ນັກຄົ້ນຄວ້າເຊື່ອວ່າ, ໃນ vivo, ການເຮັດໃຫ້ປົກກະຕິຂອງ autophagy ປະສົມປະສານຫລີກລ້ຽງການສະສົມຂອງຄວາມເສຍຫາຍ intracellular ແລະປ້ອງກັນການຫຼຸດລົງຂອງອາຍຸແລະການເຮັດວຽກຂອງຈຸລັງດາວທຽມ.ເຖິງແມ່ນວ່າຢູ່ໃນຈຸລັງລໍາຕົ້ນຂອງມະນຸດຜູ້ສູງອາຍຸ, ເຊັ່ນ: ບໍ່ດົນມານີ້, Parrish ແລະ Rodes ຍັງໄດ້ປະກອບສ່ວນທີ່ສໍາຄັນ, ສະແດງໃຫ້ເຫັນເຖິງທ່າແຮງຕ້ານການອັກເສບຂອງ PRP.ໃນເວລານີ້, ຈຸດສຸມແມ່ນກ່ຽວກັບການພົວພັນລະຫວ່າງ platelets ແລະ neutrophils.ໃນການສືບສວນຂອງພວກເຂົາ, ນັກຄົ້ນຄວ້າໄດ້ອະທິບາຍວ່າ platelets activated ທີ່ປ່ອຍອອກມາໂດຍອາຊິດ arachidonic ໄດ້ຖືກດູດຊຶມໂດຍ neutrophils ແລະປ່ຽນເປັນ leukotrienes ແລະ prostaglandins, ເຊິ່ງເປັນໂມເລກຸນອັກເສບທີ່ຮູ້ຈັກ.ຢ່າງໃດກໍຕາມ, ປະຕິສໍາພັນ neutrophil platelet ອະນຸຍາດໃຫ້ leukotriene ທີ່ຈະປ່ຽນເປັນ lipoproteins, ທີ່ໄດ້ຮັບການພິສູດວ່າເປັນທາດໂປຼຕີນຈາກຕ້ານການອັກເສບປະສິດທິພາບທີ່ສາມາດຈໍາກັດການກະຕຸ້ນຂອງ neutrophils ແລະປ້ອງກັນ dialysis, ແລະສົ່ງເສີມການສືບທອດໄປສູ່ຂັ້ນຕອນສຸດທ້າຍຂອງ cascade ການປິ່ນປົວ.
ສະພາບແວດລ້ອມຈຸນລະພາກ proinflammatory ແຊກແຊງຂະບວນການປິ່ນປົວ.ຄວາມສັບສົນຫຼາຍແມ່ນວ່າກິດຈະກໍາ protease ສູງ inhibits ການປະຕິບັດທໍາມະຊາດຂອງປັດໄຈການຂະຫຍາຍຕົວ (GF).ນອກເຫນືອໄປຈາກຄຸນສົມບັດ mitotic, angiogenic ແລະ chemotactic ຂອງມັນ, PRP ຍັງເປັນແຫຼ່ງທີ່ອຸດົມສົມບູນຂອງປັດໃຈການຂະຫຍາຍຕົວຫຼາຍ.ຊີວະໂມເລກຸນເຫຼົ່ານີ້ອາດຈະຕ້ານຜົນກະທົບທີ່ເປັນອັນຕະລາຍໃນເນື້ອເຍື່ອອັກເສບໂດຍການຄວບຄຸມການອັກເສບທີ່ເພີ່ມຂຶ້ນແລະການສ້າງຕັ້ງການກະຕຸ້ນ anabolic.
ປັດໄຈຈຸລັງ
Cytokines ໃນ PRP ມີບົດບາດສໍາຄັນໃນການຈັດການຂະບວນການສ້ອມແປງເນື້ອເຍື່ອແລະຄວບຄຸມຄວາມເສຍຫາຍອັກເສບ.cytokines ຕ້ານການອັກເສບແມ່ນລະດັບຄວາມກ້ວາງຂອງໂມເລກຸນຊີວະເຄມີທີ່ໄກ່ເກ່ຍການຕອບສະຫນອງຂອງ cytokines proinflammatory, induced ຕົ້ນຕໍໂດຍ macrophages activated.cytokines ຕ້ານການອັກເສບພົວພັນກັບ inhibitors cytokine ສະເພາະແລະ receptors cytokine ທີ່ລະລາຍເພື່ອຄວບຄຸມການອັກເສບ.Interleukin (IL) – 1 receptor antagonists, IL-4, IL-10, IL-11 ແລະ IL-13 ຖືກຈັດປະເພດເປັນຢາຕ້ານການອັກເສບຕົ້ນຕໍ, cytokines.ອີງຕາມປະເພດບາດແຜທີ່ແຕກຕ່າງກັນ, ບາງ cytokines, ເຊັ່ນ: interferon, leukemia inhibitory factor, TGF- βແລະ IL-6, ເຊິ່ງສາມາດສະແດງໃຫ້ເຫັນຜົນກະທົບ proinflammatory ຫຼືຕ້ານການອັກເສບ.TNF- α, IL-1 ແລະ IL-18 ມີຕົວຮັບ cytokine ທີ່ແນ່ນອນ, ເຊິ່ງອາດຈະຍັບຍັ້ງຜົນກະທົບ proinflammatory ຂອງທາດໂປຼຕີນອື່ນໆ [37].IL-10 ແມ່ນ ໜຶ່ງ ໃນ cytokines ຕ້ານການອັກເສບທີ່ມີປະສິດທິພາບທີ່ສຸດ, ເຊິ່ງສາມາດຄວບຄຸມ cytokines proinflammatory ເຊັ່ນ IL-1, IL-6 ແລະ TNF- α, ແລະຄວບຄຸມປັດໃຈຕ້ານການອັກເສບ.ກົນໄກການຕ້ານການເຫຼົ່ານີ້ມີບົດບາດສໍາຄັນໃນການຜະລິດແລະຫນ້າທີ່ຂອງ cytokines proinflammatory.ນອກຈາກນັ້ນ, cytokines ບາງຢ່າງອາດຈະກະຕຸ້ນການຕອບສະຫນອງສັນຍານສະເພາະເພື່ອກະຕຸ້ນ fibroblasts, ເຊິ່ງເປັນສິ່ງສໍາຄັນສໍາລັບການສ້ອມແປງເນື້ອເຍື່ອ.cytokine ອັກເສບ TGF β 1, IL-1 β, IL-6, IL-13 ແລະ IL-33 ກະຕຸ້ນ fibroblasts ເພື່ອແຍກຄວາມແຕກຕ່າງຂອງ myofibroblasts ແລະປັບປຸງ ECM [38].ໃນທາງກັບກັນ, fibroblasts secrete cytokine TGF- β, IL-1 β, IL-33, CXC ແລະ CC chemokines ສົ່ງເສີມການຕອບສະຫນອງອັກເສບໂດຍການກະຕຸ້ນແລະການທົດແທນຈຸລັງພູມຕ້ານທານເຊັ່ນ macrophages.ຈຸລັງອັກເສບເຫຼົ່ານີ້ມີບົດບາດຫຼາຍໃນບາດແຜ, ສ່ວນໃຫຍ່ແມ່ນການສົ່ງເສີມການລ້າງບາດແຜ - ແລະການສັງເຄາະທາງຊີວະພາບຂອງ chemokines, metabolites ແລະປັດໃຈການຂະຫຍາຍຕົວ, ເຊິ່ງເປັນສິ່ງສໍາຄັນສໍາລັບການສ້າງເນື້ອເຍື່ອໃຫມ່.ດັ່ງນັ້ນ, cytokines ໃນ PRP ມີບົດບາດສໍາຄັນໃນການກະຕຸ້ນປະເພດຂອງເຊນ mediated ການຕອບສະຫນອງຂອງພູມຕ້ານທານແລະສົ່ງເສີມການ regression ຂອງຂັ້ນຕອນຂອງການອັກເສບ.ໃນຄວາມເປັນຈິງ, ນັກຄົ້ນຄວ້າບາງຄົນໄດ້ແຕ່ງຕັ້ງຂະບວນການນີ້ເປັນ "ການອັກເສບຟື້ນຟູ", ຊີ້ໃຫ້ເຫັນວ່າຂັ້ນຕອນຂອງການອັກເສບ, ເຖິງວ່າຈະມີຄວາມກັງວົນຂອງຄົນເຈັບ, ເປັນຂັ້ນຕອນທີ່ຈໍາເປັນແລະສໍາຄັນສໍາລັບການສະຫລຸບສົບຜົນສໍາເລັດຂອງຂະບວນການສ້ອມແປງເນື້ອເຍື່ອ, ພິຈາລະນາກົນໄກ epigenetic ສັນຍານການອັກເສບ. ສົ່ງເສີມການສຕິກຂອງເຊນ.
ບົດບາດຂອງ cytokines ໃນການອັກເສບຜິວຫນັງຂອງ fetal ແມ່ນມີຄວາມສໍາຄັນຢ່າງຫຼວງຫຼາຍຕໍ່ການຄົ້ນຄວ້າຂອງຢາປົວພະຍາດ regenerative.ຄວາມແຕກຕ່າງລະຫວ່າງກົນໄກການປິ່ນປົວຂອງ fetal ແລະຜູ້ໃຫຍ່ແມ່ນວ່າເນື້ອເຍື່ອ fetal ທີ່ເສຍຫາຍບາງຄັ້ງກໍ່ກັບຄືນສູ່ສະພາບເດີມຕາມອາຍຸຂອງ fetal ແລະປະເພດເນື້ອເຍື່ອທີ່ກ່ຽວຂ້ອງ.ໃນມະນຸດ, ຜິວຫນັງຂອງ fetal ສາມາດຟື້ນຟູຢ່າງສົມບູນພາຍໃນ 24 ອາທິດ, ໃນຂະນະທີ່ຢູ່ໃນຜູ້ໃຫຍ່, ການປິ່ນປົວບາດແຜສາມາດນໍາໄປສູ່ການສ້າງຮອຍແປ້ວ.ດັ່ງທີ່ພວກເຮົາຮູ້, ເມື່ອປຽບທຽບກັບເນື້ອເຍື່ອທີ່ມີສຸຂະພາບດີ, ຄຸນສົມບັດກົນຈັກຂອງແພຈຸລັງຮອຍແປ້ວແມ່ນຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ, ແລະຫນ້າທີ່ຂອງພວກມັນຖືກຈໍາກັດ.ຄວາມສົນໃຈໂດຍສະເພາະແມ່ນຈ່າຍໃຫ້ກັບ cytokine IL-10, ເຊິ່ງພົບວ່າມີການສະແດງອອກສູງໃນນ້ໍາ amniotic ແລະຜິວຫນັງຂອງ fetal, ແລະໄດ້ຮັບການພິສູດວ່າມີບົດບາດໃນການສ້ອມແປງຜິວຫນັງຂອງ fetal ທີ່ບໍ່ມີຮອຍແປ້ວ, ສົ່ງເສີມໂດຍຜົນກະທົບ pleiotropic ຂອງ cytokine.ZgheibC et al.ການຖ່າຍທອດຜິວຫນັງຂອງ fetal ເຂົ້າໄປໃນຫນູ transgenic knockout (KO) IL-10 ແລະຫນູຄວບຄຸມໄດ້ຖືກສຶກສາ.ຫນູ IL-10KO ສະແດງໃຫ້ເຫັນອາການອັກເສບແລະການສ້າງຮອຍແປ້ວປະມານ grafts, ໃນຂະນະທີ່ grafts ໃນກຸ່ມຄວບຄຸມບໍ່ສະແດງໃຫ້ເຫັນການປ່ຽນແປງທີ່ສໍາຄັນໃນຄຸນສົມບັດທາງຊີວະພາບແລະບໍ່ມີການປິ່ນປົວບາດແຜ.
ຄວາມສໍາຄັນຂອງການຄວບຄຸມຄວາມດຸ່ນດ່ຽງທີ່ລະອຽດອ່ອນລະຫວ່າງການສະແດງອອກຂອງ cytokines ຕ້ານການອັກເສບແລະ pro-inflammatory ແມ່ນວ່າສຸດທ້າຍ, ເມື່ອການຜະລິດເກີນ, ໃນທີ່ສຸດຈະສົ່ງສັນຍານຂອງການເຊື່ອມໂຊມຂອງເຊນໂດຍການຫຼຸດຜ່ອນການສະແດງອອກຂອງ genes ທີ່ແນ່ນອນ.ຕົວຢ່າງ, ໃນຢາປົວພະຍາດ musculoskeletal, IL-1 β Down ຄວບຄຸມ SOX9, ເຊິ່ງມີຄວາມຮັບຜິດຊອບຕໍ່ການພັດທະນາກະດູກອ່ອນ.SOX9 ຜະລິດປັດໄຈການຖ່າຍທອດທີ່ສໍາຄັນສໍາລັບການພັດທະນາຂອງກະດູກອ່ອນ, ຄວບຄຸມປະເພດຂອງ collagen alpha 1 (Col2A1), ແລະຮັບຜິດຊອບສໍາລັບການເຂົ້າລະຫັດພັນທຸກໍາຂອງ collagen ປະເພດ II.IL-1 β ສຸດທ້າຍ, ການສະແດງອອກຂອງ Col2A1 ແລະ aggrecan ໄດ້ຫຼຸດລົງ.ຢ່າງໃດກໍ່ຕາມ, ການປິ່ນປົວທີ່ມີຜະລິດຕະພັນທີ່ອຸດົມສົມບູນຂອງ platelet ໄດ້ຖືກສະແດງໃຫ້ເຫັນເຖິງການຍັບຍັ້ງ IL-1 β ມັນຍັງເປັນພັນທະມິດທີ່ເປັນໄປໄດ້ຂອງຢາຟື້ນຟູເພື່ອຮັກສາການສະແດງອອກຂອງພັນທຸກໍາຂອງ collagen ແລະຫຼຸດຜ່ອນ apoptosis ຂອງ chondrocytes ທີ່ຖືກກະຕຸ້ນໂດຍ cytokines proinflammatory.
ການກະຕຸ້ນ Anabolic: ນອກເຫນືອຈາກການຄວບຄຸມການອັກເສບຂອງເນື້ອເຍື່ອທີ່ເສຍຫາຍ, cytokines ໃນ PRP ຍັງມີສ່ວນຮ່ວມໃນປະຕິກິລິຍາ anabolic ໂດຍການຫຼີ້ນບົດບາດຂອງພວກເຂົາຂອງ mitosis, ການດຶງດູດທາງເຄມີແລະການຂະຫຍາຍພັນ.ນີ້ແມ່ນການສຶກສາໃນ vitro ນໍາໂດຍ Cavallo et al.ເພື່ອສຶກສາຜົນກະທົບຂອງ PRPs ທີ່ແຕກຕ່າງກັນກ່ຽວກັບ chondrocytes ຂອງມະນຸດ.ນັກຄົ້ນຄວ້າໄດ້ສັງເກດເຫັນວ່າຜະລິດຕະພັນ PRP ທີ່ມີຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ແລະຄວາມເຂັ້ມຂົ້ນຂອງ leukocyte ຂ້ອນຂ້າງກະຕຸ້ນການເຄື່ອນໄຫວຂອງ chondrocyte ປົກກະຕິ, ເຊິ່ງເຫມາະສົມສໍາລັບການສົ່ງເສີມບາງກົນໄກຂອງຈຸລັງຂອງການຕອບສະຫນອງ anabolic.ຕົວຢ່າງ, ການສະແດງອອກຂອງ collagen ປະເພດ ii ແລະ glycans ລວມໄດ້ຖືກສັງເກດເຫັນ.ໃນທາງກົງກັນຂ້າມ, ຄວາມເຂັ້ມຂຸ້ນສູງຂອງ platelets ແລະ leukocytes ເບິ່ງຄືວ່າຈະກະຕຸ້ນເສັ້ນທາງສັນຍານຂອງຈຸລັງອື່ນໆທີ່ກ່ຽວຂ້ອງກັບ cytokines ຕ່າງໆ.ຜູ້ຂຽນແນະນໍາວ່ານີ້ອາດຈະເປັນຍ້ອນການມີເມັດເລືອດຂາວຈໍານວນຫລາຍໃນສູດ PRP ໂດຍສະເພາະນີ້.ຈຸລັງເຫຼົ່ານີ້ເບິ່ງຄືວ່າມີຄວາມຮັບຜິດຊອບຕໍ່ການສະແດງອອກຂອງປັດໃຈການຂະຫຍາຍຕົວບາງຢ່າງເຊັ່ນ VEGF, FGF-b, ແລະ interleukins IL-1b ແລະ IL-6, ເຊິ່ງອາດຈະກະຕຸ້ນ TIMP-1 ແລະ IL-10.ໃນຄໍາສັບຕ່າງໆອື່ນໆ, ເມື່ອປຽບທຽບກັບສູດ PRP ທີ່ "ບໍ່ດີ", ການປະສົມ PRP ທີ່ອຸດົມສົມບູນໃນ platelets ແລະເມັດເລືອດຂາວເບິ່ງຄືວ່າຈະສົ່ງເສີມການບຸກລຸກຂອງ chondrocytes.
ການສຶກສາທີ່ອອກແບບໂດຍ Schnabel et al.ໄດ້ຖືກອອກແບບເພື່ອປະເມີນບົດບາດຂອງວັດສະດຸຊີວະພາບ autologous ໃນເນື້ອເຍື່ອ tendon ມ້າ.ຜູ້ຂຽນໄດ້ເກັບກໍາຕົວຢ່າງເລືອດແລະ tendon ຈາກຫົກມ້າຜູ້ໃຫຍ່ໄວຫນຸ່ມ (2-4 ປີ), ແລະໄດ້ສຸມໃສ່ການສຶກສາຮູບແບບການສະແດງອອກຂອງ gene, DNA ແລະເນື້ອໃນ collagen ຂອງການຂະຫຍາຍຕົວ tendon ຂອງ flexor digitorum superficialis ຂອງມ້າທີ່ລ້ຽງຢູ່ໃນຂະຫນາດກາງທີ່ມີ PRP. ຫຼືຜະລິດຕະພັນເລືອດອື່ນໆ.ການປູກຝັງເສັ້ນເອັນໄດ້ຖືກປູກຝັງຢູ່ໃນເລືອດ, plasma, PRP, platelet deficiency plasma (PPP) ຫຼື bone marrow aspirates (BMA), ແລະອາຊິດ amino ໄດ້ຖືກເພີ່ມເຂົ້າໄປໃນ 100%, 50% ຫຼື 10% serum ທີ່ບໍ່ມີ DMEM.ໃນການດໍາເນີນງານການວິເຄາະທາງຊີວະເຄມີທີ່ໃຊ້ໄດ້ຫຼັງຈາກ ..., ນັກຄົ້ນຄວ້າໄດ້ສັງເກດເຫັນວ່າ TGF- βຄວາມເຂັ້ມຂົ້ນຂອງ PDGF-BB ແລະ PDGF-1 ໃນ PRP ຂະຫນາດກາງແມ່ນສູງກວ່າໂດຍສະເພາະຂອງຜະລິດຕະພັນເລືອດອື່ນໆທີ່ທົດສອບ.ນອກຈາກນັ້ນ, ເນື້ອເຍື່ອ tendon ທີ່ລ້ຽງຢູ່ໃນຂະຫນາດກາງ 100% PRP ສະແດງໃຫ້ເຫັນການສະແດງອອກຂອງ gene ເພີ່ມຂຶ້ນຂອງທາດໂປຼຕີນຈາກ matrix COL1A1, COL3A1 ແລະ COMP, ແຕ່ບໍ່ໄດ້ເພີ່ມ enzymes catabolic MMPs3 ແລະ 13. ຢ່າງຫນ້ອຍໃນແງ່ຂອງໂຄງສ້າງ tendon, ນີ້ໃນການສຶກສາ vivo ສະຫນັບສະຫນູນການນໍາໃຊ້. autolo - ຜະລິດຕະພັນເລືອດ gouty, ຫຼື PRP, ສໍາລັບການປິ່ນປົວຂອງ tendinitis mammalian ຂະຫນາດໃຫຍ່.
Chen et al.ຜົນກະທົບຂອງການຟື້ນຟູຂອງ PRP ໄດ້ຖືກປຶກສາຫາລືຕື່ມອີກ.ໃນການສຶກສາທີ່ຜ່ານມາຂອງພວກເຂົາ, ນັກຄົ້ນຄວ້າໄດ້ພິສູດວ່າ, ນອກເຫນືອຈາກການເສີມສ້າງໂຄງສ້າງຂອງກະດູກອ່ອນ, PRP ຍັງສົ່ງເສີມການເພີ່ມຂື້ນຂອງການສັງເຄາະ ECM ແລະຍັບຍັ້ງປະຕິກິລິຢາອັກເສບຂອງ cartilage articular ແລະ nucleus pulposus.PRP ສາມາດກະຕຸ້ນ TGF ຜ່ານ phosphorylation ຂອງ Smad2 / 3- βເສັ້ນທາງສັນຍານມີບົດບາດສໍາຄັນໃນການເຕີບໂຕຂອງເຊນແລະຄວາມແຕກຕ່າງ.ນອກຈາກນັ້ນ, ມັນຍັງເຊື່ອກັນວ່າເສັ້ນເລືອດຕັນໃນ fibrin ສ້າງຕັ້ງຂຶ້ນຫຼັງຈາກການກະຕຸ້ນ PRP ສະຫນອງໂຄງສ້າງສາມມິຕິທີ່ແຂງ, ເຮັດໃຫ້ຈຸລັງສາມາດຍຶດຫມັ້ນ, ເຊິ່ງອາດຈະນໍາໄປສູ່ການສ້າງເນື້ອເຍື່ອໃຫມ່.
ນັກຄົ້ນຄວ້າອື່ນໆໄດ້ປະກອບສ່ວນທີ່ສໍາຄັນໃນການປິ່ນປົວບາດແຜຜິວຫນັງຊໍາເຮື້ອໃນດ້ານການແພດຜິວຫນັງ.ນີ້ກໍ່ເປັນທີ່ຫນ້າສັງເກດ.ສໍາລັບຕົວຢ່າງ, ການຄົ້ນຄວ້າທີ່ດໍາເນີນໂດຍ Hessler ແລະ Shyam ໃນປີ 2019 ສະແດງໃຫ້ເຫັນວ່າ PRP ມີມູນຄ່າເປັນການປິ່ນປົວທາງເລືອກທີ່ເປັນໄປໄດ້ແລະມີປະສິດທິພາບ, ໃນຂະນະທີ່ບາດແຜຊໍາເຮື້ອທີ່ທົນທານຕໍ່ຢາຍັງນໍາພາລະເສດຖະກິດທີ່ສໍາຄັນຕໍ່ການດູແລສຸຂະພາບ.ໂດຍສະເພາະ, ບາດແຜຕີນຂອງພະຍາດເບົາຫວານແມ່ນເປັນບັນຫາສຸຂະພາບທີ່ສໍາຄັນທີ່ມີຊື່ສຽງ, ເຊິ່ງເຮັດໃຫ້ແຂນຂາຖືກຕັດອອກໄດ້ງ່າຍ.ການສຶກສາທີ່ຈັດພີມມາໂດຍ Ahmed et al.ໃນປີ 2017 ສະແດງໃຫ້ເຫັນວ່າ autologous PRP gel ສາມາດກະຕຸ້ນການປິ່ນປົວບາດແຜໃນຄົນເຈັບທີ່ມີບາດແຜຕີນຂອງພະຍາດເບົາຫວານຊໍາເຮື້ອໂດຍການປ່ອຍປັດໃຈການຂະຫຍາຍຕົວທີ່ຈໍາເປັນ, ດັ່ງນັ້ນການປັບປຸງອັດຕາການປິ່ນປົວຢ່າງຫຼວງຫຼາຍ.ເຊັ່ນດຽວກັນ, Gonchar ແລະເພື່ອນຮ່ວມງານໄດ້ທົບທວນຄືນແລະປຶກສາຫາລືກ່ຽວກັບທ່າແຮງການຟື້ນຟູຂອງ PRP ແລະການຂະຫຍາຍຕົວຂອງ cocktails ໃນການປັບປຸງການປິ່ນປົວບາດແຜຕີນຂອງພະຍາດເບົາຫວານ.ນັກຄົ້ນຄວ້າໄດ້ສະເຫນີວ່າການນໍາໃຊ້ການຜະສົມຂອງປັດໄຈການຂະຫຍາຍຕົວມີແນວໂນ້ມທີ່ຈະເປັນການແກ້ໄຂທີ່ເປັນໄປໄດ້, ເຊິ່ງສາມາດປັບປຸງຄວາມໄດ້ປຽບຂອງການນໍາໃຊ້ PRP ແລະປັດໄຈການຂະຫຍາຍຕົວດຽວ.ດັ່ງນັ້ນ, ເມື່ອປຽບທຽບກັບການນໍາໃຊ້ປັດໄຈການຂະຫຍາຍຕົວດຽວ, ການປະສົມປະສານຂອງ PRP ແລະກົນລະຍຸດການປິ່ນປົວອື່ນໆອາດຈະສົ່ງເສີມການປິ່ນປົວບາດແຜຊໍາເຮື້ອຢ່າງຫຼວງຫຼາຍ.
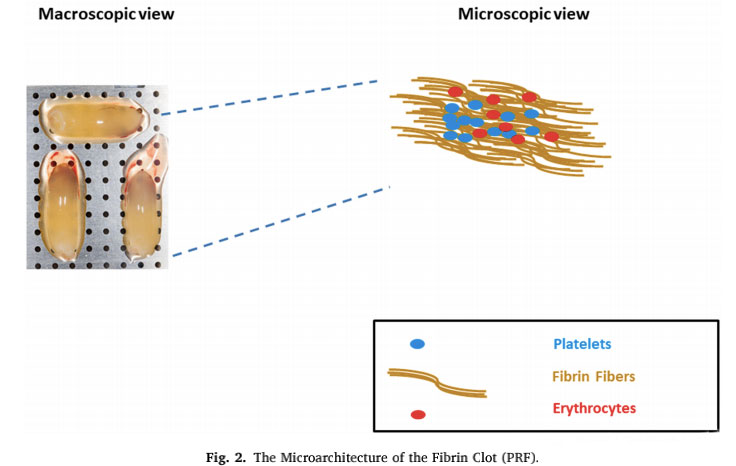
Fibrin
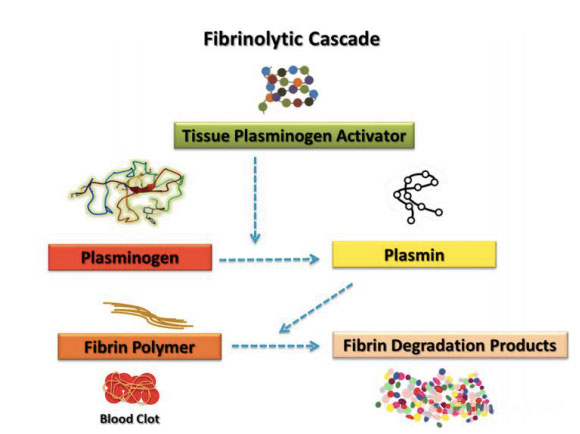
Platelets ມີປັດໃຈຈໍານວນຫນຶ່ງທີ່ກ່ຽວຂ້ອງກັບລະບົບ fibrinolytic, ເຊິ່ງອາດຈະເຮັດໃຫ້ປະຕິກິລິຍາ fibrinolytic ຄວບຄຸມຫຼືຫຼຸດລົງ.ການພົວພັນທີ່ໃຊ້ເວລາແລະການປະກອບສ່ວນພີ່ນ້ອງຂອງອົງປະກອບ hematological ແລະການທໍາງານຂອງ platelet ໃນການເຊື່ອມໂຊມຂອງກ້າມແມ່ນຍັງເປັນບັນຫາທີ່ສົມຄວນຂອງການສົນທະນາຢ່າງກວ້າງຂວາງໃນຊຸມຊົນ.ວັນນະຄະດີແນະນໍາການສຶກສາຈໍານວນຫຼາຍທີ່ສຸມໃສ່ພຽງແຕ່ platelets, ທີ່ມີຊື່ສຽງສໍາລັບຄວາມສາມາດທີ່ຈະສົ່ງຜົນກະທົບຕໍ່ຂະບວນການປິ່ນປົວ.ເຖິງວ່າຈະມີການສຶກສາທີ່ຍັງຄ້າງຄາຈໍານວນຫລາຍ, ອົງປະກອບ hematological ອື່ນໆ, ເຊັ່ນ: ປັດໃຈ coagulation ແລະລະບົບ fibrinolytic, ຍັງໄດ້ຖືກພົບເຫັນວ່າປະກອບສ່ວນຢ່າງຫຼວງຫຼາຍຕໍ່ການສ້ອມແປງບາດແຜທີ່ມີປະສິດທິຜົນ.ຕາມຄໍານິຍາມ, fibrinolysis ແມ່ນຂະບວນການທາງຊີວະພາບທີ່ສັບສົນທີ່ຂຶ້ນກັບການກະຕຸ້ນຂອງ enzymes ບາງຢ່າງເພື່ອສົ່ງເສີມການເຊື່ອມໂຊມຂອງ fibrin.ປະຕິກິລິຍາ Fibrinolysis ໄດ້ຖືກສະເຫນີໂດຍຜູ້ຂຽນອື່ນໆວ່າຜະລິດຕະພັນການຍ່ອຍສະຫຼາຍຂອງ fibrin (fdp) ອາດຈະເປັນຕົວແທນໂມເລກຸນທີ່ຮັບຜິດຊອບສໍາລັບການກະຕຸ້ນການສ້ອມແປງເນື້ອເຍື່ອ.ລໍາດັບເຫດການທາງຊີວະວິທະຍາທີ່ສໍາຄັນກ່ອນຫນ້າແມ່ນມາຈາກການຝາກ fibrin ແລະການໂຍກຍ້າຍຂອງ angiogenesis, ເຊິ່ງເປັນສິ່ງຈໍາເປັນສໍາລັບການປິ່ນປົວບາດແຜ.ການສ້າງກ້ອນຫີນຫຼັງຈາກການບາດເຈັບເຮັດຫນ້າທີ່ເປັນຊັ້ນປ້ອງກັນເພື່ອປົກປ້ອງເນື້ອເຍື່ອຈາກການສູນເສຍເລືອດແລະການຮຸກຮານຂອງຕົວແທນຈຸລິນຊີ, ແລະຍັງສະຫນອງ matrix ຊົ່ວຄາວທີ່ຈຸລັງສາມາດເຄື່ອນຍ້າຍໃນລະຫວ່າງຂະບວນການສ້ອມແປງ.ກ້າມແມ່ນເນື່ອງມາຈາກ fibrinogen ໄດ້ຖືກຕັດໂດຍ serine protease, ແລະ platelets ໄດ້ຖືກລວບລວມຢູ່ໃນຕາຫນ່າງເສັ້ນໄຍ fibrin ຂ້າມເຊື່ອມຕໍ່.ປະຕິກິລິຢານີ້ເຮັດໃຫ້ເກີດການ polymerization ຂອງ fibrin monomer, ເຊິ່ງເປັນເຫດການຕົ້ນຕໍຂອງການສ້າງກ້ອນເລືອດ.clot ຍັງສາມາດຖືກນໍາໃຊ້ເປັນອ່າງເກັບນຂອງ cytokines ແລະປັດໄຈການຂະຫຍາຍຕົວ, ທີ່ຖືກປ່ອຍອອກມາໃນລະຫວ່າງການ degranulation ຂອງ platelets activated.ລະບົບ fibrinolytic ຖືກຄວບຄຸມຢ່າງເຂັ້ມງວດໂດຍ plasmin, ແລະມີບົດບາດສໍາຄັນໃນການສົ່ງເສີມການເຄື່ອນຍ້າຍຂອງເຊນ, ຊີວະພາບຂອງປັດໃຈການຂະຫຍາຍຕົວແລະລະບຽບການຂອງລະບົບ protease ອື່ນໆທີ່ກ່ຽວຂ້ອງກັບການອັກເສບແລະການຟື້ນຟູຂອງຈຸລັງ.ອົງປະກອບທີ່ສໍາຄັນຂອງ fibrinolysis, ເຊັ່ນ urokinase plasminogen activator receptor (uPAR) ແລະ plasminogen activator inhibitor-1 (PAI-1), ເປັນທີ່ຮູ້ຈັກທີ່ຈະສະແດງອອກໃນ mesenchymal stem cells (MSCs), ເຊິ່ງເປັນປະເພດເຊນພິເສດທີ່ຈໍາເປັນສໍາລັບການປິ່ນປົວບາດແຜທີ່ປະສົບຜົນສໍາເລັດ. .
ການເຄື່ອນຍ້າຍເຊນ
ການກະຕຸ້ນຂອງ plasminogen ໂດຍຜ່ານສະມາຄົມ uPA uPAR ແມ່ນຂະບວນການທີ່ສົ່ງເສີມການເຄື່ອນຍ້າຍຂອງຈຸລັງອັກເສບເນື່ອງຈາກວ່າມັນເສີມຂະຫຍາຍ proteolysis extracellular.ເນື່ອງຈາກການຂາດ transmembrane ແລະໂດເມນ intracellular, uPAR ຕ້ອງການ co receptors ເຊັ່ນ integrin ແລະ vitellin ເພື່ອຄວບຄຸມການເຄື່ອນຍ້າຍຂອງເຊນ.ມັນຊີ້ໃຫ້ເຫັນຕື່ມອີກວ່າການຜູກມັດຂອງ uPA uPAR ເຮັດໃຫ້ເກີດຄວາມໃກ້ຊິດຂອງ uPAR ສໍາລັບ vitrectonectin ແລະ integrin, ເຊິ່ງສົ່ງເສີມການຍຶດຫມັ້ນຂອງເຊນ.Plasminogen activator inhibitor-1 (PAI-1) ໃນທາງກັບກັນເຮັດໃຫ້ຈຸລັງແຍກອອກ.ເມື່ອມັນຜູກມັດກັບ uPA ຂອງ uPA upar integrin complex ຢູ່ດ້ານຂອງເຊລ, ມັນຈະທໍາລາຍການພົວພັນລະຫວ່າງ upar vitellin ແລະ integrin integrin.
ໃນສະພາບການຂອງຢາປົວພະຍາດ regenerative, ຈຸລັງລໍາຕົ້ນຂອງກະດູກ mesenchymal ໄດ້ຖືກລະດົມຈາກໄຂກະດູກໃນກໍລະນີຂອງຄວາມເສຍຫາຍຂອງອະໄວຍະວະຮ້າຍແຮງ, ດັ່ງນັ້ນເຂົາເຈົ້າອາດຈະພົບເຫັນຢູ່ໃນການໄຫຼວຽນຂອງຄົນເຈັບທີ່ມີກະດູກຫັກຫຼາຍ.ຢ່າງໃດກໍ່ຕາມ, ໃນກໍລະນີສະເພາະ, ເຊັ່ນຄວາມລົ້ມເຫຼວຂອງຫມາກໄຂ່ຫຼັງໃນຂັ້ນຕອນສຸດທ້າຍ, ຄວາມລົ້ມເຫຼວຂອງຕັບໃນຂັ້ນຕອນສຸດທ້າຍ, ຫຼືໃນລະຫວ່າງການປະຕິເສດຫຼັງຈາກການປ່ຽນຫົວໃຈ, ຈຸລັງເຫຼົ່ານີ້ອາດຈະບໍ່ຖືກກວດພົບໃນເລືອດ [66].ຫນ້າສົນໃຈ, ໄຂກະດູກຂອງມະນຸດເຫຼົ່ານີ້ມາຈາກຈຸລັງ progenitor mesenchymal (stromal) ບໍ່ສາມາດກວດພົບໃນເລືອດຂອງບຸກຄົນທີ່ມີສຸຂະພາບດີ [67].ບົດບາດຂອງ uPAR ໃນການລະດົມຈຸລັງລໍາຕົ້ນ mesenchymal ກະດູກ (BMSCs) ໄດ້ຖືກສະເຫນີກ່ອນຫນ້ານີ້, ເຊິ່ງຄ້າຍຄືກັບການເກີດຂື້ນຂອງ uPAR ໃນການລະດົມຈຸລັງລໍາຕົ້ນຂອງ hematopoietic (HSCs).Varabaneni et al.ຜົນໄດ້ຮັບສະແດງໃຫ້ເຫັນວ່າການນໍາໃຊ້ປັດໄຈການກະຕຸ້ນ granulocyte colony ໃນຫນູທີ່ຂາດແຄນ uPAR ເຮັດໃຫ້ເກີດຄວາມລົ້ມເຫຼວຂອງ MSC, ເຊິ່ງອີກເທື່ອຫນຶ່ງເຮັດໃຫ້ບົດບາດສະຫນັບສະຫນູນຂອງລະບົບ fibrinolysis ໃນການເຄື່ອນຍ້າຍຂອງເຊນ.ການສຶກສາເພີ່ມເຕີມຍັງສະແດງໃຫ້ເຫັນວ່າ glycosyl phosphatidylinositol ຍຶດເອົາຕົວຮັບ uPA ຄວບຄຸມການຍຶດຕິດ, ການເຄື່ອນຍ້າຍ, ການຂະຫຍາຍຕົວແລະຄວາມແຕກຕ່າງໂດຍການກະຕຸ້ນເສັ້ນທາງສັນຍານ intracellular ບາງຢ່າງ, ດັ່ງຕໍ່ໄປນີ້: phosphatidylinositol 4,5-diphosphate 3-kt, ແລະ kiningdhases / A. (FAK).
ໃນສະພາບການຂອງການປິ່ນປົວບາດແຜຂອງ MSC, ປັດໃຈ fibrinolytic ໄດ້ພິສູດຄວາມສໍາຄັນຕື່ມອີກ.ຕົວຢ່າງ, ຫນູທີ່ຂາດ plasminogen ສະແດງໃຫ້ເຫັນຄວາມລ່າຊ້າທີ່ຮ້າຍແຮງໃນການປິ່ນປົວບາດແຜ, ສະແດງໃຫ້ເຫັນວ່າ plasmin ມີຄວາມສໍາຄັນໃນຂະບວນການນີ້.ໃນມະນຸດ, ການສູນເສຍ plasmin ຍັງສາມາດເຮັດໃຫ້ເກີດອາການແຊກຊ້ອນຂອງການປິ່ນປົວບາດແຜ.ການຂັດຂວາງການໄຫຼວຽນຂອງເລືອດສາມາດຍັບຍັ້ງການເກີດໃຫມ່ຂອງເນື້ອເຍື່ອຢ່າງຫຼວງຫຼາຍ, ເຊິ່ງຍັງອະທິບາຍວ່າເປັນຫຍັງຂະບວນການຟື້ນຟູເຫຼົ່ານີ້ແມ່ນທ້າທາຍຫຼາຍໃນຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານ.
ຈຸລັງລໍາຕົ້ນ mesenchymal ໄຂກະດູກໄດ້ຖືກບັນຈຸໄປຫາສະຖານທີ່ບາດແຜເພື່ອເລັ່ງການປິ່ນປົວບາດແຜ.ພາຍໃຕ້ເງື່ອນໄຂທີ່ຫມັ້ນຄົງ, ຈຸລັງເຫຼົ່ານີ້ສະແດງອອກ uPAuPAR ແລະ PAI-1.ທາດໂປຼຕີນຈາກສອງອັນສຸດທ້າຍແມ່ນປັດໃຈ hypoxia inducible α (HIF-1 α) ການກໍາຫນົດເປົ້າຫມາຍແມ່ນສະດວກຫຼາຍເພາະວ່າ HIF-1 ໃນ MSCs αການກະຕຸ້ນຂອງ FGF-2 ແລະ HGF ໄດ້ສົ່ງເສີມການຂຶ້ນກົດລະບຽບຂອງ FGF-2 ແລະ HGF;HIF-2 α ໃນທາງກັບກັນ, VEGF-A [77] ແມ່ນຂຶ້ນລະບຽບ, ເຊິ່ງຮ່ວມກັນປະກອບສ່ວນໃນການປິ່ນປົວບາດແຜ,.ນອກຈາກນັ້ນ, HGF ເບິ່ງຄືວ່າຈະເສີມຂະຫຍາຍການທົດແທນຈຸລັງລໍາຕົ້ນຂອງກະດູກ mesenchymal ເຂົ້າໄປໃນສະຖານທີ່ບາດແຜໃນລັກສະນະ synergistic.ມັນຕ້ອງໄດ້ຮັບການສັງເກດເຫັນວ່າສະພາບ ischemic ແລະ hypoxic ໄດ້ຖືກສະແດງໃຫ້ເຫັນການແຊກແຊງຢ່າງຫຼວງຫຼາຍຕໍ່ການສ້ອມແປງບາດແຜ.ເຖິງແມ່ນວ່າ BMSCs ມີແນວໂນ້ມທີ່ຈະອາໄສຢູ່ໃນເນື້ອເຍື່ອທີ່ສະຫນອງລະດັບອົກຊີເຈນທີ່ຕໍ່າ, ການຢູ່ລອດຂອງ BMSCs ທີ່ຖືກຖ່າຍທອດໃນ vivo ກາຍເປັນຈໍາກັດເພາະວ່າຈຸລັງທີ່ຖືກປູກຝັງມັກຈະຕາຍພາຍໃຕ້ເງື່ອນໄຂທີ່ບໍ່ດີທີ່ສັງເກດເຫັນໃນເນື້ອເຍື່ອທີ່ເສຍຫາຍ.ຊະຕາກໍາຂອງການຍຶດຕິດແລະການຢູ່ລອດຂອງຈຸລັງລໍາຕົ້ນຂອງກະດູກ mesenchymal ພາຍໃຕ້ hypoxia ແມ່ນຂຶ້ນກັບປັດໃຈ fibrinolytic secreted ໂດຍຈຸລັງເຫຼົ່ານີ້.PAI-1 ມີຄວາມຜູກພັນສູງສໍາລັບ vitellin, ດັ່ງນັ້ນມັນສາມາດແຂ່ງຂັນສໍາລັບການຜູກມັດຂອງ uPAR ແລະ integrin ກັບ vitellin, ດັ່ງນັ້ນການຍັບຍັ້ງການຍຶດຕິດຂອງເຊນແລະການເຄື່ອນຍ້າຍ.
Monocyte ແລະລະບົບການຟື້ນຟູ
ອີງຕາມວັນນະຄະດີ, ມີການສົນທະນາຫຼາຍກ່ຽວກັບບົດບາດຂອງ monocytes ໃນການປິ່ນປົວບາດແຜ.Macrophages ສ່ວນໃຫຍ່ແມ່ນມາຈາກ monocytes ເລືອດແລະມີບົດບາດສໍາຄັນໃນການຟື້ນຟູຢາປົວພະຍາດ [81].ເນື່ອງຈາກວ່າ neutrophils secrete IL-4, IL-1, IL-6 ແລະ TNF- α, ຈຸລັງເຫຼົ່ານີ້ປົກກະຕິແລ້ວເຈາະເຂົ້າໄປໃນບາດແຜປະມານ 24-48 ຊົ່ວໂມງຫຼັງຈາກການບາດເຈັບ.Platelets ປ່ອຍ thrombin ແລະ platelet factor 4 (PF4), ເຊິ່ງສາມາດສົ່ງເສີມການທົດແທນຂອງ monocytes ແລະແຕກຕ່າງກັນເຂົ້າໄປໃນ macrophages ແລະຈຸລັງ dendritic.ຄຸນນະສົມບັດທີ່ສໍາຄັນຂອງ macrophages ແມ່ນ plasticity ຂອງເຂົາເຈົ້າ, ນັ້ນແມ່ນ, ພວກເຂົາສາມາດປ່ຽນ phenotypes ແລະແຕກຕ່າງກັນເຂົ້າໄປໃນປະເພດຈຸລັງອື່ນໆ, ເຊັ່ນ: ຈຸລັງ endothelial, ແລະຫຼັງຈາກນັ້ນສະແດງຫນ້າທີ່ທີ່ແຕກຕ່າງກັນກັບ stimuli biochemical ທີ່ແຕກຕ່າງກັນໃນ microenvironment ຂອງບາດແຜ.ຈຸລັງອັກເສບສະແດງອອກສອງ phenotypes ທີ່ສໍາຄັນ, M1 ຫຼື M2, ຂຶ້ນກັບສັນຍານໂມເລກຸນທ້ອງຖິ່ນເປັນແຫຼ່ງຂອງການກະຕຸ້ນ.M1 macrophages ແມ່ນ induced ໂດຍຕົວແທນຈຸລິນຊີ, ສະນັ້ນພວກເຂົາເຈົ້າມີຜົນກະທົບ proinflammatory ຫຼາຍ.ໃນທາງກົງກັນຂ້າມ, M2 macrophages ປົກກະຕິແລ້ວແມ່ນຜະລິດໂດຍປະຕິກິລິຍາປະເພດ 2 ແລະມີຄຸນສົມບັດຕ້ານການອັກເສບ, ໂດຍປົກກະຕິມີລັກສະນະເພີ່ມຂຶ້ນຂອງ IL-4, IL-5, IL-9, ແລະ IL-13.ມັນຍັງມີສ່ວນຮ່ວມໃນການສ້ອມແປງເນື້ອເຍື່ອໂດຍຜ່ານການຜະລິດປັດໃຈການຂະຫຍາຍຕົວ.ການຫັນປ່ຽນຈາກປະເພດຍ່ອຍ M1 ຫາ M2 ສ່ວນໃຫຍ່ແມ່ນຂັບເຄື່ອນໂດຍຂັ້ນຕອນຂອງການປິ່ນປົວບາດແຜ.M1 macrophages ກະຕຸ້ນ neutrophil apoptosis ແລະລິເລີ່ມການລ້າງຈຸລັງເຫຼົ່ານີ້).phagocytosis ຂອງ neutrophils ກະຕຸ້ນກິດຈະກໍາຫຼາຍໆຢ່າງ, ເຊິ່ງການຜະລິດ cytokines ຖືກປິດ, macrophages polarizing ແລະປ່ອຍ TGF- β 1. ປັດໄຈການຂະຫຍາຍຕົວນີ້ແມ່ນຕົວຄວບຄຸມທີ່ສໍາຄັນຂອງຄວາມແຕກຕ່າງຂອງ myofibroblast ແລະການຫົດຕົວຂອງບາດແຜ, ເຊິ່ງອະນຸຍາດໃຫ້ແກ້ໄຂການອັກເສບແລະ. ການເລີ່ມຕົ້ນຂອງໄລຍະ proliferation ໃນ cascade ການປິ່ນປົວ [57].ທາດໂປຼຕີນອີກອັນຫນຶ່ງທີ່ກ່ຽວຂ້ອງກັບຂະບວນການຂອງເຊນແມ່ນ serine (SG).ຈຸລັງ hemopoietic secretory granule proteoglycan ໄດ້ຖືກພົບເຫັນວ່າມີຄວາມຈໍາເປັນໃນການເກັບຮັກສາທາດໂປຼຕີນຈາກ secretory ໃນຈຸລັງພູມຕ້ານທານສະເພາະ, ເຊັ່ນ: ຈຸລັງ mast, neutrophils ແລະ cytotoxic T lymphocytes.ເຖິງແມ່ນວ່າຈຸລັງທີ່ບໍ່ແມ່ນ hematopoietic ຈໍານວນຫຼາຍຍັງສັງເຄາະ plasminogen, ຈຸລັງອັກເສບທັງຫມົດຜະລິດທາດໂປຼຕີນຈາກຈໍານວນຫຼວງຫຼາຍແລະເກັບຮັກສາໄວ້ໃນເມັດເພື່ອປະຕິສໍາພັນກັບຜູ້ໄກ່ເກ່ຍອັກເສບອື່ນໆ, ລວມທັງ proteases, cytokines, chemokines ແລະປັດໃຈການຂະຫຍາຍຕົວ.ຕ່ອງໂສ້ glycosaminoglycan (GAG) ທີ່ຖືກຄິດຄ່າທໍານຽມທາງລົບໃນ SG ເບິ່ງຄືວ່າມີຄວາມສໍາຄັນຕໍ່ຄວາມຫມັ້ນຄົງຂອງເມັດ secretory, ຍ້ອນວ່າພວກເຂົາສາມາດຜູກມັດແລະອໍານວຍຄວາມສະດວກໃນການເກັບຮັກສາອົງປະກອບເມັດທີ່ມີຄ່າທີ່ສໍາຄັນໃນຈຸລັງ, ທາດໂປຼຕີນ, ແລະລະບົບຕ່ອງໂສ້ GAG ສະເພາະ.ກ່ຽວກັບການເຂົ້າຮ່ວມຂອງເຂົາເຈົ້າໃນການຄົ້ນຄວ້າ PRP, Woulfe ແລະເພື່ອນຮ່ວມງານໄດ້ສະແດງໃຫ້ເຫັນກ່ອນຫນ້ານີ້ວ່າການຂາດ SG ແມ່ນກ່ຽວຂ້ອງຢ່າງໃກ້ຊິດກັບການປ່ຽນແປງ morphological platelet;Platelet factor 4 β- ຂໍ້ບົກພ່ອງຂອງການເກັບຮັກສາ PDGF ໃນ thromboglobulin ແລະ platelets;ການລວມຕົວຂອງ platelet ບໍ່ດີ ແລະຄວາມລັບໃນ vitro ແລະ thrombosis ຜິດປົກກະຕິໃນ vivo.ດັ່ງນັ້ນ, ນັກຄົ້ນຄວ້າໄດ້ສະຫຼຸບວ່າ proteoglycan ນີ້ເບິ່ງຄືວ່າເປັນຕົວຄວບຄຸມຕົ້ນຕໍຂອງ thrombosis.
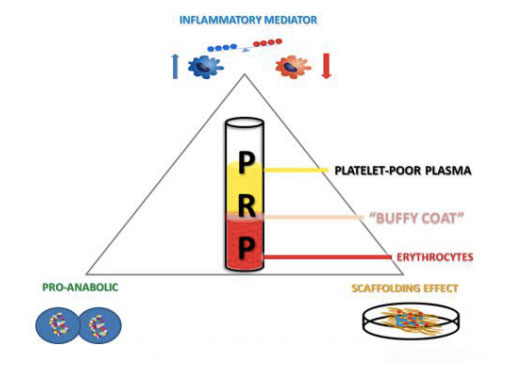
ຜະລິດຕະພັນທີ່ອຸດົມສົມບູນຂອງ Platelet ສາມາດໄດ້ຮັບເລືອດທັງຫມົດສ່ວນບຸກຄົນໂດຍຜ່ານການເກັບກໍາແລະການ centrifugation, ແລະແບ່ງສ່ວນປະສົມເຂົ້າໄປໃນຊັ້ນຕ່າງໆທີ່ມີ plasma, platelets, ເມັດເລືອດຂາວແລະເມັດເລືອດຂາວ.ເມື່ອຄວາມເຂັ້ມຂຸ້ນຂອງ platelet ສູງກວ່າມູນຄ່າພື້ນຖານ, ມັນສາມາດເລັ່ງການເຕີບໂຕຂອງກະດູກແລະເນື້ອເຍື່ອອ່ອນ, ມີຜົນຂ້າງຄຽງຫນ້ອຍທີ່ສຸດ.ຄໍາຮ້ອງສະຫມັກຂອງຜະລິດຕະພັນ PRP autologous ເປັນເຕັກໂນໂລຊີຊີວະພາບຂ້ອນຂ້າງໃຫມ່, ເຊິ່ງໄດ້ສະແດງໃຫ້ເຫັນຢ່າງຕໍ່ເນື່ອງຜົນໄດ້ຮັບ optimistic ໃນການກະຕຸ້ນແລະເສີມຂະຫຍາຍການປິ່ນປົວຂອງການບາດເຈັບຂອງເນື້ອເຍື່ອຕ່າງໆ.ປະສິດທິພາບຂອງວິທີການປິ່ນປົວທາງເລືອກນີ້ອາດຈະໄດ້ຮັບການສະຫນອງທ້ອງຖິ່ນຂອງລະດັບຄວາມກ້ວາງຂອງປັດໃຈການຂະຫຍາຍຕົວແລະທາດໂປຼຕີນເພື່ອຈໍາລອງແລະສະຫນັບສະຫນູນຂະບວນການປິ່ນປົວບາດແຜ physiological ແລະການສ້ອມແປງເນື້ອເຍື່ອ.ນອກຈາກນັ້ນ, ລະບົບ fibrinolytic ແນ່ນອນມີອິດທິພົນທີ່ສໍາຄັນຕໍ່ການສ້ອມແປງເນື້ອເຍື່ອທັງຫມົດ.ນອກເຫນືອໄປຈາກການປ່ຽນແປງການທົດແທນຈຸລັງຂອງຈຸລັງອັກເສບແລະຈຸລັງລໍາຕົ້ນ mesenchymal ໄຂກະດູກ, ມັນຍັງສາມາດຄວບຄຸມກິດຈະກໍາ proteolytic ຂອງພື້ນທີ່ປິ່ນປົວບາດແຜແລະຂະບວນການຟື້ນຟູຂອງເນື້ອເຍື່ອ mesodermal, ລວມທັງກະດູກ, cartilage ແລະກ້າມຊີ້ນ, ສະນັ້ນມັນເປັນອົງປະກອບທີ່ສໍາຄັນຂອງ. ຢາປົວພະຍາດ musculoskeletal.
ການປິ່ນປົວແບບເລັ່ງດ່ວນແມ່ນເປົ້າຫມາຍທີ່ດໍາເນີນການສູງໂດຍຜູ້ຊ່ຽວຊານດ້ານການແພດຈໍານວນຫຼາຍ.PRP ເປັນຕົວແທນຂອງເຄື່ອງມືທາງຊີວະພາບໃນທາງບວກ, ເຊິ່ງຍັງສືບຕໍ່ສະຫນອງການພັດທະນາທີ່ດີໃນການກະຕຸ້ນແລະການປະສານງານຂອງ cascade ຂອງເຫດການ regenerative.ຢ່າງໃດກໍຕາມ, ເນື່ອງຈາກວ່າເຄື່ອງມືການປິ່ນປົວນີ້ຍັງສະລັບສັບຊ້ອນຫຼາຍ, ໂດຍສະເພາະແມ່ນເນື່ອງຈາກວ່າມັນປ່ອຍປັດໄຈທາງຊີວະພາບນັບບໍ່ຖ້ວນແລະກົນໄກການປະຕິສໍາພັນຕ່າງໆຂອງເຂົາເຈົ້າແລະຜົນກະທົບ transduction ສັນຍານ, ການຄົ້ນຄວ້າເພີ່ມເຕີມແມ່ນຈໍາເປັນ.
(ເນື້ອໃນຂອງບົດຄວາມນີ້ຖືກພິມຄືນ, ແລະພວກເຮົາບໍ່ໄດ້ສະຫນອງການຮັບປະກັນຄວາມຖືກຕ້ອງ, ຄວາມຫນ້າເຊື່ອຖືຫຼືຄວາມສົມບູນຂອງເນື້ອໃນທີ່ມີຢູ່ໃນບົດຄວາມນີ້, ແລະບໍ່ຮັບຜິດຊອບຕໍ່ຄວາມຄິດເຫັນຂອງບົດຄວາມນີ້, ກະລຸນາເຂົ້າໃຈ.)
ເວລາປະກາດ: 16-12-2022